一针持久降尿酸3-6个月的siRNA新药申报临床;默沙东口服降血脂多肽达3期临床终点……
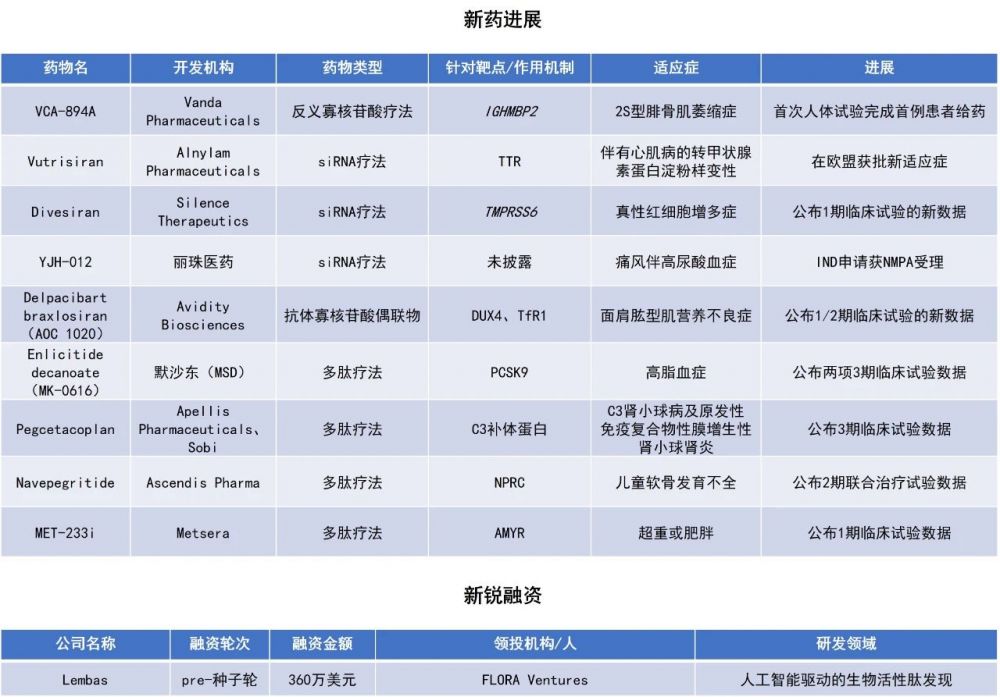
近期,全球多肽和寡核苷酸(TIDES)领域迎来系列进展。Alnylam Pharmaceuticals公司的小干扰RNA(siRNA)疗法Amvuttra(vutrisiran)在欧盟获批新适应症。Apellis Pharmaceuticals公司与Sobi公司的双环肽疗法pegcetacoplan的3期临床试验结果积极,第26周时关键指标下降近70%。默沙东(MSD)用于治疗高脂血症的在研口服环肽疗法enlicitide decanoate的两项3期临床试验达到主要终点和所有关键次要终点。丽珠医药用于治疗痛风的siRNA疗法YJH-012的IND申请获中国国家药品监督管理局(NMPA)正式受理,该疗法单次给药有望实现3-6个月的持续降尿酸效果。
Vutrisiran:在欧盟获批新适应症
Alnylam Pharmaceuticals公司宣布,欧盟委员会(EC)已批准其siRNA疗法Amvuttra用于治疗伴有心肌病的转甲状腺素蛋白淀粉样变性(ATTR-CM)患者。根据新闻稿,这一批准使Amvuttra成为获得EC批准可用于治疗ATTR-CM及遗传性转甲状腺素蛋白介导(hATTR)淀粉样变性的多发性神经病(polyneuropathy)的首个RNAi疗法。
此次批准主要基于关键3期HELIOS-B研究的积极结果。该研究为一项随机、双盲、安慰剂对照的多中心全球试验。分析显示,Amvuttra在总体和单药治疗人群中均达成所有10项预设的主要与次要终点,显著降低全因死亡与复发性心血管事件,同时改善6分钟步行距离、健康状态、生活质量(KCCQ评分)以及心力衰竭症状与严重程度(NYHA分级)。在总体人群中,与安慰剂相比,Amvuttra在主要复合终点(全因死亡和复发性心血管事件)方面实现了28%的风险降低。在一项预设的次要终点分析中,包括最长36个月的双盲期及6个月的开放标签延长期,该患者群体的死亡率显著下降了36%,进一步印证其临床益处。
Pegcetacoplan:公布3期临床试验数据
Apellis Pharmaceuticals公司与Sobi公司公布了其3期VALIANT研究开放标签期的新数据,该试验评估Empaveli(pegcetacoplan)在治疗C3肾小球病(C3G)及原发性免疫复合物性膜增生性肾小球肾炎(IC-MPGN)中的疗效与安全性。Empaveli是一款靶向C3补体蛋白的聚乙二醇化(PEGylated)双环肽疗法。双环肽分子集抗体、小分子药物及肽类的特性于一身,具有与抗体类似的亲和性和精确的靶向特异性;同时,由于它们分子量较小,使得其能够快速深入地渗透组织。此前,Empaveli已获FDA批准用于治疗阵发性睡眠性血红蛋白尿症(PNH)和由年龄相关性黄斑变性(AMD)引起的地图样萎缩(GA)。
结果显示,与安慰剂相比,Empaveli在第26周实现了蛋白尿下降达68%,差异具有统计学意义。这一疗效在治疗持续一年后仍得以维持。同时,接受Empaveli治疗的患者在估算肾小球滤过率(eGFR)指标上显示出肾功能的持续稳定。Empaveli整体安全性良好,耐受性与既往研究结果一致,未发现新的安全性信号,支持其在该类补体介导性肾病中的持续开发潜力。美国FDA与欧洲药品管理局(EMA)正在对该药物用于肾病的监管申请进行审评。
Enlicitide decanoate(MK-0616):公布两项3期临床试验数据
默沙东(MSD)公司宣布,其在研口服PCSK9抑制剂enlicitide decanoate(MK-0616)在三项3期临床试验中的前两项取得积极结果,显示该疗法能有效用于治疗正在接受降脂治疗(包括至少使用他汀类药物)的高脂血症成人患者。PCSK9是一种经验证用以降低低密度脂蛋白胆固醇(LDL-C)的靶标。然而,目前尚无口服PCSK9抑制剂可供医生和患者使用。Enlicitide decanoate是一种与PCSK9结合并抑制PCSK9与LDL受体相互作用的大环肽,旨在通过与目前获批的注射型PCSK9抑制剂相同的生物学机制降低LDL-C,但以每日片剂形式给药。根据新闻稿,enlicitide decanoate有望成为获美国FDA批准的首款口服PCSK9抑制剂。
此次公布的结果显示,CORALreef HeFH和CORALreef AddOn试验均成功达到主要终点和所有关键次要终点。与安慰剂(CORALreef HeFH)或其他口服非他汀类药物(CORALreef AddOn)相比,enlicitide decanoate在降低患者的LDL-C水平方面具有统计学显著性和临床意义的改善。此外,在两项研究中使用该疗法患者的不良事件和严重不良事件(SAE)的发生率,与对照组相较在临床上无显著差异。
MET-233i:公布1期临床试验数据
Metsera公司公布了其超长效、每月皮下注射的胰淀素类似物MET-233i的1期临床试验的积极结果。在该研究中,接受MET-233i治疗的患者在第36天时实现了平均8.4%的安慰剂校正体重减轻效果。在临床试验中观察到MET-233i的半衰期长达19天,支持每月一次给药,并且耐受性良好,未出现安全性信号。
此外,MET-233i经过工程优化,可以与Metsera公司的超长效GLP-1受体激动剂MET-097i在溶液中稳定共存(具有匹配的溶解参数和相似的观察半衰期)。MET-233i单药以及与MET-097i联用的临床研究目前正在进行中。
Delpacibart braxlosiran(AOC 1020):公布1/2期临床试验的新数据
Avidity Biosciences公司公布了其用于治疗面肩肱型肌营养不良症(FSHD)的在研抗体寡核苷酸偶联物(AOC)delpacibart
braxlosiran(del-brax)在临床1/2期试验FORTITUDE中的积极新数据。FSHD是由于DUX4基因异常表达所引起。DUX4蛋白的异常表达导致肌肉细胞基因表达的变化,造成FSHD患者肌肉功能的终身、渐进性丧失。根据新闻稿,del-brax是首个旨在治疗FSHD根本原因的在研AOC疗法,由一种专有的转铁蛋白受体1(TfR1)靶向单克隆抗体,与靶向DUX4 mRNA的siRNA偶联所组成。
此次公布的结果显示,与安慰剂相比,在接受del-brax治疗的FSHD患者中观察到肌肉功能活动能力、肌肉力量和患者报告的结局(PROs)衡量的生活质量方面的改善,并且生物标志物出现了快速而显著的下降。安全性方面,del-brax表现出良好的长期安全性和耐受性,大多数不良事件为轻度或中度,无相关的严重不良事件,也没有停药事件。
VCA-894A:首次人体试验完成首例患者给药
Vanda Pharmaceuticals公司宣布,其反义寡核苷酸(ASO)疗法VCA-894A的首次人体临床试验已完成首例患者给药。VCA-894A是一种2'-O-甲氧基乙基(MOE)硫代磷酸寡核苷酸钠盐,特异性靶向IGHMBP2基因中一种剪接位点变体,该变体会导致2S型腓骨肌萎缩症(CMT2S)。
YJH-012:IND申请获NMPA受理
丽珠医药宣布,其1类创新药YJH-012的IND申请已于近日获NMPA正式受理。该药物是一款以GalNAc为递送系统的siRNA疗法,旨在精准递送siRNA至尿酸合成的主要场所——肝脏,降低关键致病蛋白的生成量,从源头上长效抑制尿酸生成,有望治疗痛风伴高尿酸血症。新闻稿指出,YJH-012单次给药即可实现3-6个月的持续降尿酸效果。此外,尿酸抑制平稳上升并长期维持,避免治疗初期尿酸急速下降将导致“溶晶反应”从而引发二次痛风,相对现有治疗药物,具备更好的治疗潜力。安全性方面,在临床前研究中,未观察到次黄嘌呤、IMP、AMP、GMP等关键嘌呤代谢物的异常升高,也未发现肝脏相关病理性改变,初步提示了良好的安全性特征。
