默沙东收购Verona Pharma:COPD药物研发,动物模型如何赋能?
7月9日,美国制药巨头默沙东对外宣布将以约100亿美元收购专注于呼吸系统疾病的英国生物制药公司Verona Pharma,通过此次收购,默沙东将获得Verona Pharma的慢性阻塞性肺疾病治疗药物 OhtuvayreTM(药物名:Ensifentrine),用于加强其慢性阻塞性肺病(COPD)治疗药物管线。

图片来源:MSD官网
Ensifentrine是一种首创的选择性磷酸二酯酶3和4(PDE3和PDE4)双重抑制剂,通过抑制PDE3升高cAMP,舒张气道平滑肌,而同时抑制PDE4减少炎性细胞激活与迁移,兼具支气管扩张和非甾体抗炎作用,用于成人慢性阻塞性肺病(COPD)的维持治疗[1]。该药于2024年6月获得美国食品药品监督管理局(FDA)批准,是二十多年来首个用于COPD治疗的全新吸入机制药物。目前,该药也在临床试验中评估用于治疗非囊性纤维化支气管扩张症。有预测显示,到2030年代中期,该药物年销售额最高或达到近40亿美元。
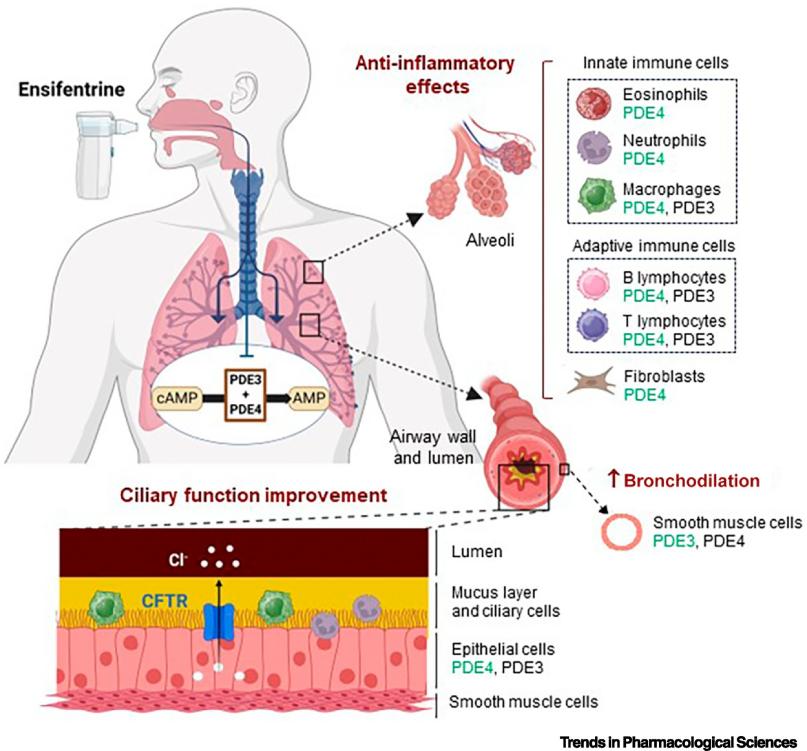
慢性阻塞性肺病(Chronic Obstructive Pulmonary Disease,COPD),常简称为慢阻肺,是一种异质性肺病,其特征在于由气道异常(支气管炎、细支气管炎)和/或肺泡异常(肺气肿)所致的慢性呼吸道症状(呼吸困难、咳嗽、痰产生和/或恶化),引起持续的、通常进行性的气流受限[2]。其最常见的病因是香烟烟雾,其他风险因素包括接触职业粉尘和化学品、空气污染和遗传因素(如alpha1-抗胰蛋白酶缺乏)。据WHO数据显示,COPD是全球第四大死因,2021年造成350万人死亡,约占全球死亡总数的5%。由于持续暴露于风险因素和世界人口老龄化的结合,预计COPD患病率和负担将在未来几十年持续增加。COPD作为国家高度关注的慢性呼吸道疾病,被列为“健康中国2030”行动计划的重点防治项目,2024年9月被纳入国家基本公共卫生服务项目,其用药市场存在巨大需求。
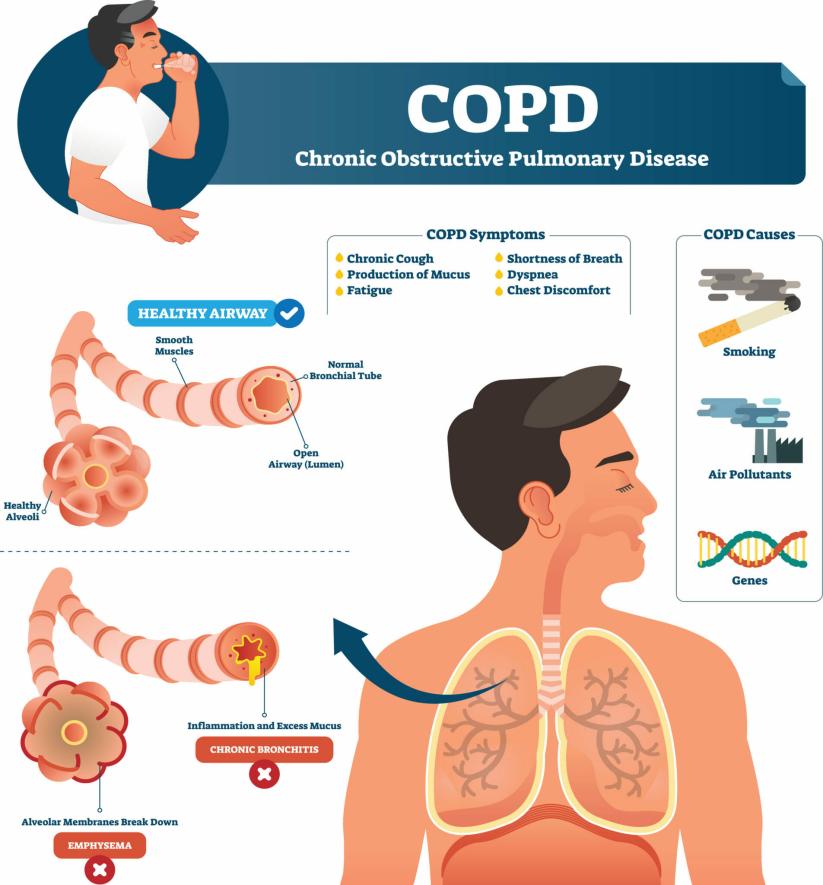
图片来源:Dr. Amit Patel
目前COPD的发病机制尚未完全阐明。慢性气道炎症、氧化应激和蛋白酶/抗蛋白酶失衡所诱发的肺组织损伤是COPD发病机制中关键因素。小气道(<2 mm)是COPD发展的早期改变部位,包括粘液积聚、免疫细胞浸润和气道壁增厚。上皮重编程,结合免疫和重塑反应,可能导致这种进行性反应,并导致肺气肿的发展[3]。巨噬细胞和中性粒细胞是COPD发病机制中至关重要的先天免疫细胞,与慢性炎症和肺气肿的发展有关。COPD中病理性巨噬细胞浓度增加的部分原因是氧化剂诱导的对吸烟引起的凋亡的抵抗。尽管寿命延长,但COPD相关巨噬细胞表现出对细菌和凋亡细胞的吞噬功能缺陷,导致更多炎症。这种缺陷可能是由巨噬细胞免疫代谢改变引起的,包括线粒体功能障碍和代偿性糖酵解减少。
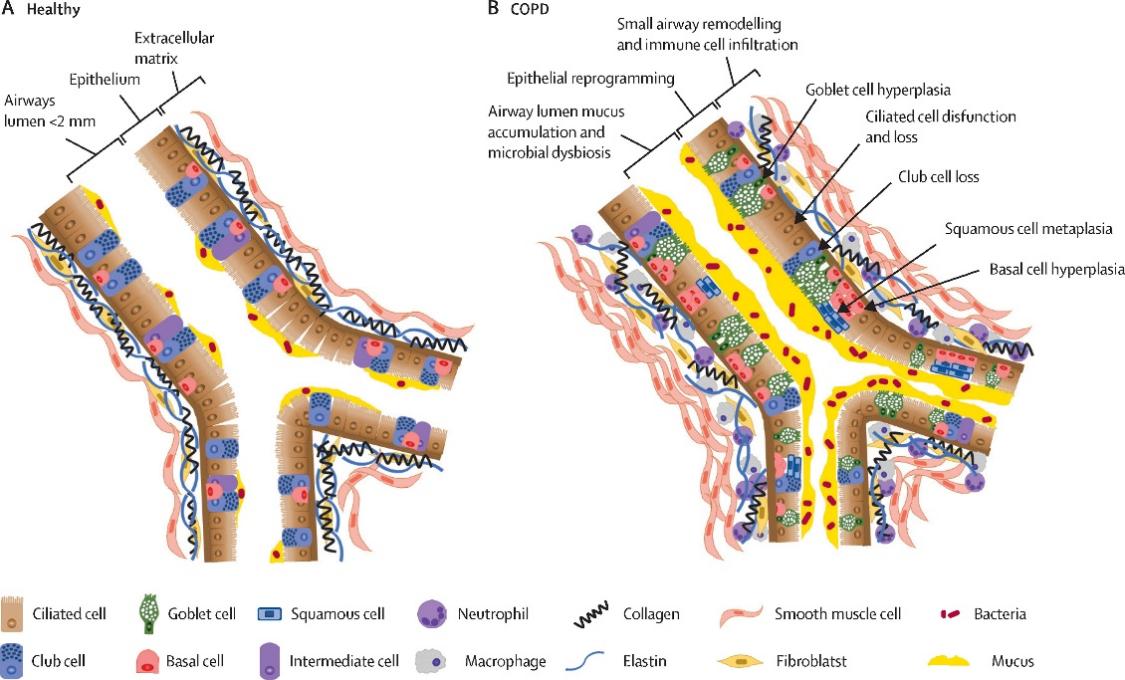
图片来源:柳叶刀
适应性免疫反应和微生物环境的变化在COPD中是至关重要的,细胞介导的适应性免疫反应将炎症导向四种主要极化反应:1型(T1;干扰素驱动,通常被认为是对病毒的反应);2型(T2;IL-4、IL-5和IL-13驱动,对蠕虫或过敏原的反应);17型(T17;IL-17和IL-22驱动,对细胞外细菌的应答);和T调节性(调节性T细胞,抗炎)。气道中T17驱动的炎症标志物增加与肺气肿、中性粒细胞炎症和对吸入性皮质类固醇(ICS)无反应有关[4,5]。T2炎症的基因组标志物与嗜酸性粒细胞(主要T2效应细胞之一)的增加和更好的ICS反应相关[6]。嗜酸性粒细胞计数是第一个添加到慢性阻塞性肺病全球倡议(GOLD)指南中的血液生物标志物,有证据表明它有助于确定ICS在有症状的患者中的作用。然而,抗IL-5生物制剂在COPD试验中未达到主要终点[7,8]。单独治疗COPD嗜酸性粒细胞炎症的有效性较低可能是由于重叠的炎症改变或不可逆的肺损伤。衰老的肺也可能更难治疗,因为竞争性的病理改变,如干细胞耗竭(导致再生能力降低)和炎症[9-11]。
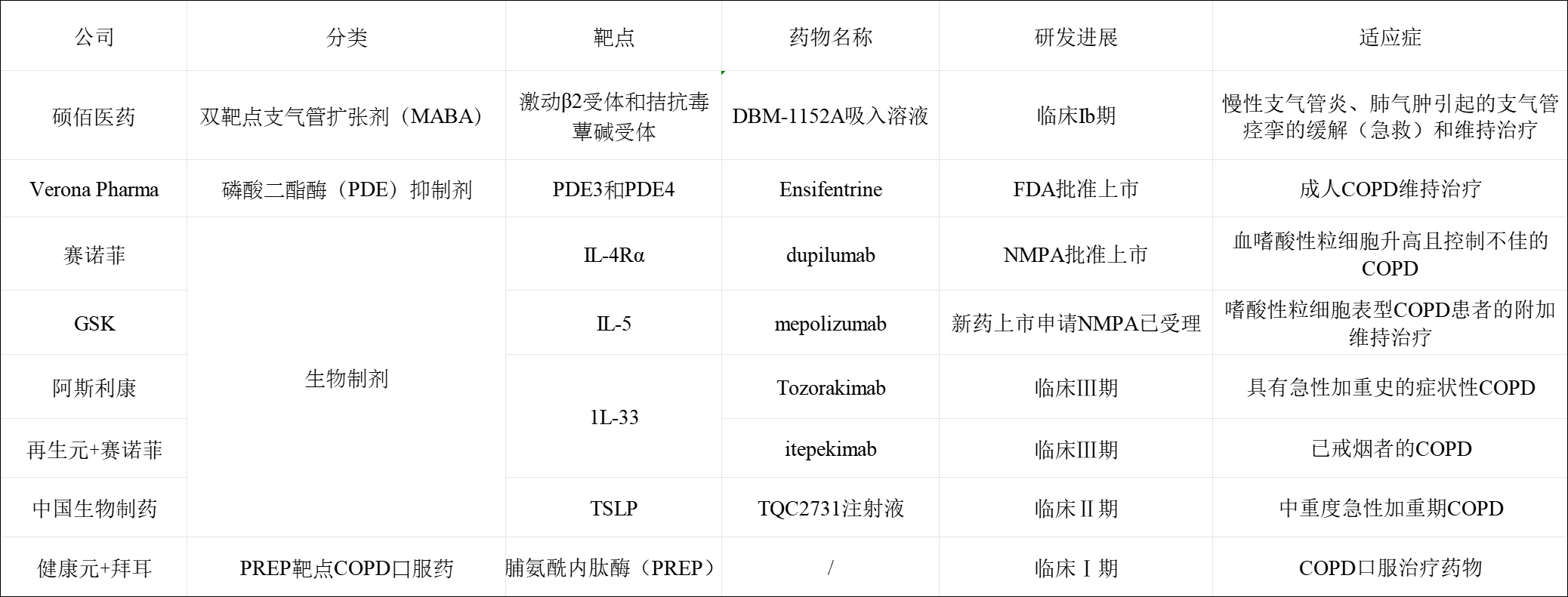
目前COPD主要在研药物靶点(公开数据整理)
作为模拟人类疾病进程、验证药物疗效及探索分子机制的核心工具,动物模型在研究中扮演着核心角色,其优化与应用是推动临床转化的关键环节。
COPD动物模型分为单因素诱导和多因素联合诱导模型,香烟(cigarette smoke,CS)、脂多糖(Lipopolysaccharide,LPS)、蛋白酶、大气污染物诱导模型和基因调控模型为常见的诱导模型,多因素联合诱导模型主要通过结合以上两种因素进行构建。吸入、滴鼻、气道内滴注、气管切开注射为常用诱导方式,根据诱导因素的不同而选择。
中洪博元COPD模型介绍:
江西中洪博元生物技术有限公司目前具有三种COPD模型,单纯吸烟诱导的小鼠慢阻肺模型、吸烟联合LPS诱导小鼠慢阻肺模型和吸烟联合LPS诱导大鼠慢阻肺模型。
香烟烟雾诱导的COPD模型可使动物出现气道炎症、黏液分泌增加、肺组织损伤等与人类吸烟导致的COPD相似的病理改变;吸烟联合LPS诱导的模型能更好地模拟人类COPD的复杂病理过程,LPS与吸烟的协同作用可使肺组织的损伤更加严重,如肺泡结构破坏、肺气肿形成、肺小叶间质增生等病理改变更为明显,有利于研究肺组织损伤机制,并且单纯吸烟诱导COPD模型耗时较长,通常需要数月时间,而LPS可激活炎症细胞,加速并加重肺部炎症及组织破坏,从而有效缩短造模时间,提高研究效率。通过观察药物对吸烟联合LPS诱导的COPD模型的炎症反应、肺功能、肺组织病理等方面的改善作用,能够更准确地评价药物的疗效,有助于揭示COPD的发病机制和药物治疗的靶点,为新药研发提供依据。
