EAE模型 | 从实验室到临床:2025MS研发如何加速转化?
多发性硬化症(MS)是一种尚无根治方法的自身免疫性神经退行性疾病,临床以“肢体无力、感觉异常、视力下降、共济失调”为主要表现,病情呈“缓解-复发”或慢性进展性发展,严重影响患者生活质量。
图源:网络
自身免疫性脑脊髓炎(EAE)是其最典型且广泛应用的动物模型,其病理特征与MS高度契合。EAE可通过主动免疫或被动输注致病性T细胞在啮齿类动物体内诱导产生,其研究进展直接助力人类MS的诊疗突破。
中洪博元EAE模型已有稳定成模效果和完善评估体系,有需要欢迎咨询。
传统治疗聚焦“抑制免疫攻击”,难以解决神经损伤不可逆的核心难题。当前MS/EAE治疗体系分层明确:
一线治疗以糖皮质激素等非特异性免疫抑制剂为主(应用占比超60%),但针对性弱;
二线为奥法妥木单抗等特异性靶点药物(难治患者应用率35%),精准性初显但适用范围有限;
整体以TNF-α等传统免疫靶点为主(占比超70%),存在15%-47%患者疗效不佳、缺乏神经修复药物的显著未满足需求。
2025年三大治疗热点+AI制药崛起,推动EAE治疗向“精准调控+主动修复”转型。
靶向Kir4.1通道:解锁髓鞘再生的“关键开关”
PART 01
2025年上海交通大学童小萍团队在《Advanced Science》发表成果,依托EAE及狨猴MS模型验证,明确候选药2-D08可解决EAE“破坏-修复”失衡痛点,为MS研发提供关键动物实验依据。
机制上,2-D08通过靶向激活少突胶质前体细胞(OPCs)的Kir4.1钾离子通道,恢复钾离子稳态、推动OPCs成熟,从根源促进髓鞘再生。利用两种动物模型验证证实其疗效:MOG35-55诱导EAE小鼠给药4周后,脱髓鞘病变缩小、神经功能评分降低40%以上;狨猴MS模型中,其可改善运动功能且无不良反应,修复效果优于临床常用药。同时,动物实验验证其具备良好血脑屏障穿透性,为中枢神经应用奠定基础。
动物实验结果证实2-D08打破传统治疗局限,为进展型MS修复带来希望。依托扎实的动物实验数据,该药物已启动临床前安全性评估,有望成为首个兼具抗炎与修复功效的MS候选药物。
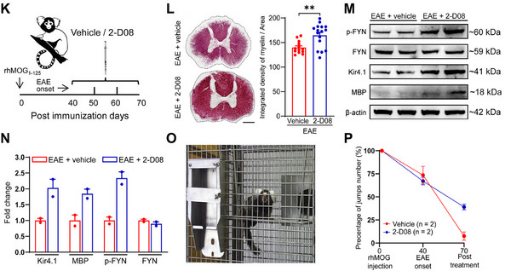
图源:Advanced Science官网
聚焦脑膜B细胞:精准阻断神经炎症的“复发开关”
PART 02
复发是MS治疗痛点,现有药物难以预防。
2025年7月,西湖大学何丹阳/徐和平团队在《Immunity》发表研究,首次锁定脑膜内自身反应性B细胞为复发核心靶点,为创新药研发明确方向。研究证实,该B细胞通过与致脑炎性T细胞结合放大炎症,且依赖B细胞MHC II分子和T细胞GM-CSF。针对性干预该靶点可显著减轻EAE复发,为药物研发提供扎实临床前数据支撑。
该靶点为MS复发预防类创新药研发打开窗口,而精准靶点验证与药物筛选离不开标准化动物模型。未来基于该靶点的抗体药、小分子抑制剂等,有望解决复发难题。
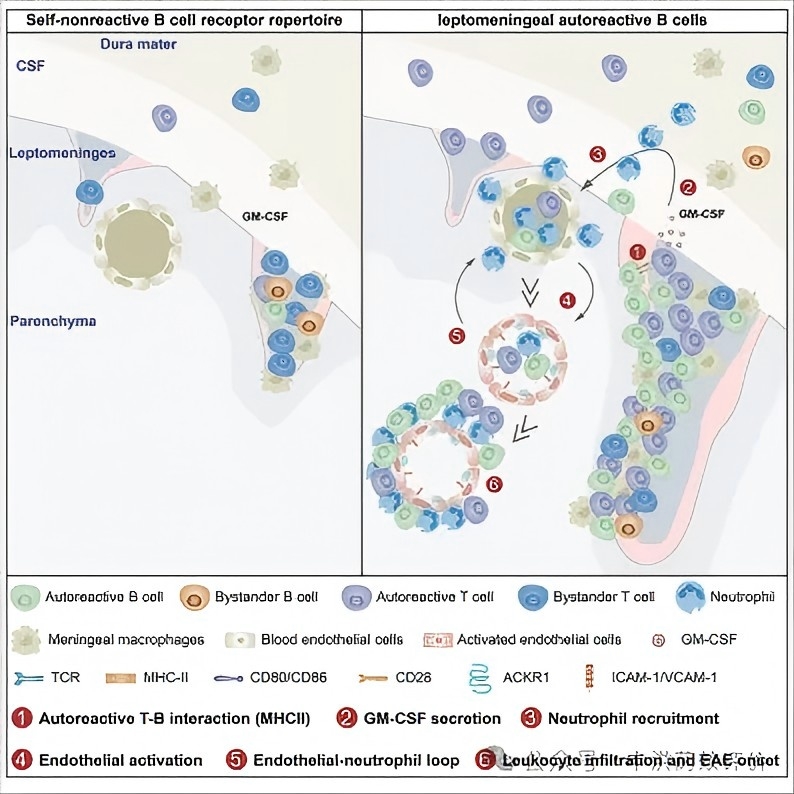
图源:Immunity官网
除了精准靶向免疫细胞与髓鞘修复的创新研发方向,从现有药物或天然产物中挖掘治疗潜力、实现“老药新用”或“天然产物现代化”,也是2025年EAE治疗研究的重要探索方向,这类研究往往具备研发周期短、安全性可控的优势,能更快推进临床转化。
中药现代化靶向:雷公藤活性成分激活PACAP/cAMP通路抗炎修复
PART 03
在天然产物现代化研发浪潮中,传统中药的精准治疗潜力备受关注。2025年4月,上海中医药大学刘静雯&郭夫江教授团队在《Journal of Ethnopharmacology》发表研究,明确了雷公藤多苷片(TGT)及其活性成分雷公藤甲素(TP)对EAE的治疗价值,为中药治MS提供新依据。
研究通过MOG35-55诱导EAE小鼠模型验证发现,TGT和TP可显著改善小鼠体重下降与神经功能障碍,减轻脊髓脱髓鞘和炎症浸润;而不含TP的制剂无疗效,明确TP是核心药效物质。机制上,TP通过上调PACAP激活cAMP信号通路,进而调控下游PI3K-AKT、NF-κB及凋亡通路,同时降低促炎因子水平、抑制致病转录因子表达,实现抗炎、抗凋亡与髓鞘修复协同作用。
该研究的创新价值在于明确了TP的核心药效地位,首次揭示PACAP/cAMP信号轴为关键机制,构建了“靶点-通路-表型”的中药现代化研究范式。依托已有临床应用基础,TGT/TP有望成为MS潜力候选药。
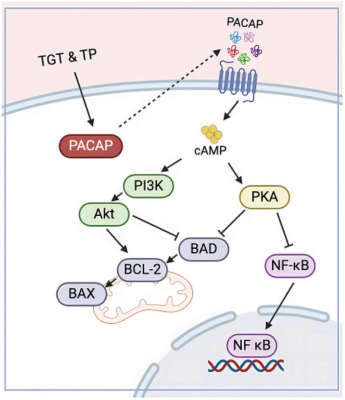
图源:Journal of Ethnopharmacology官网
AI制药赋能:助力EAE相关创新药研发
PART 04
2025年AI制药在神经免疫疾病领域应用成熟,核心赋能靶点发现、分子设计与效率提升,其技术框架可为EAE相关MS创新药研发提供支撑。
靶点挖掘上,英矽智能PandaOmics等AI平台可整合多组学数据筛选靶点,该技术可迁移应用于EAE相关研究,助力挖掘脑膜B细胞等靶点关联通路。分子设计领域,ED2Mol模型、AI设计抗炎蛋白E127Q等技术落地,可针对性优化Kir4.1通道调节剂等EAE相关候选药,大幅缩短研发周期。临床前阶段,AI可整合实验数据优化设计、预测成药性,为雷公藤甲素等评估提供支撑,减少重复实验、降低成本。
热点延伸:全球MS药物研发竞争与国内差异化机遇
全球MS药物市场规模超200亿美元且持续增长,研发聚焦“精准抗炎+神经修复”,国际与国内创新力量加速布局,核心进展如下表所示:
研发主体类型 | 代表主体/药物 | 核心信息(靶点/技术/阶段) |
国际药企 | 赛诺菲 | tolebrutinib(BTK抑制剂);nrSPMSⅢ期试验 |
Immunic公司 | vidofludimus calcium(Nurr1激活剂);Ⅱ期试验降低神经损伤标志物20% | |
罗氏 | Ocrevus(皮下注射版);已获批上市,提升患者用药便利性 | |
国内企业/团队 | 上海交大团队(候选药) | 2-D08(Kir4.1通道髓鞘再生候选药);已启动临床前安全性评估 |
驯鹿生物 | BCMA CAR-T疗法(伊基奥仑赛);改善进展型MS残疾评分,无严重神经毒性 | |
诺诚健华 | 奥布替尼(BTK抑制剂);启动MS全球Ⅲ期临床试验 | |
上海中医药大学团队 | 雷公藤甲素(TP);中药现代化成果,抗炎+修复协同作用,潜力候选药 |
回顾2025年EAE研发已转向“精准靶向+主动修复”,2-D08、脑膜B细胞靶点、雷公藤活性成分为核心突破点,AI制药提升研发效率,为MS治疗开辟新可能。基于EAE模型的研发突破带来多款MS潜力候选药,明确“个性化精准治疗”方向,有望改变MS治疗格局,惠及更多患者。
你对这些前沿治疗方向有什么疑问?欢迎在评论区留言讨论~
参考文献:
[2]Wang Y, Xu D, Liu S, et al. Cognate interaction-dependent pathogenicity of meningeal B cells drives neuroinflammation relapse. Immunity. 2025;58(9):2256-2270.e8. doi:10.1016/j.immuni.2025.06.016
[3]Wang H, Zou J, Li Y, Liu J, Guo F. Tripterygium glycoside tablets and triptolide alleviate experimental autoimmune encephalomyelitis mice involving the PACAP/cAMP signaling pathway. J Ethnopharmacol. 2025;347:119748. doi:10.1016/j.jep.2025.119748
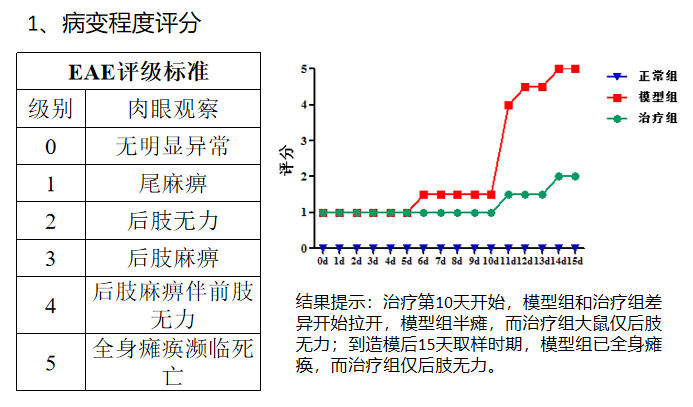
中洪博元大鼠实验性自身免疫性脑脊髓炎(EAE)模型
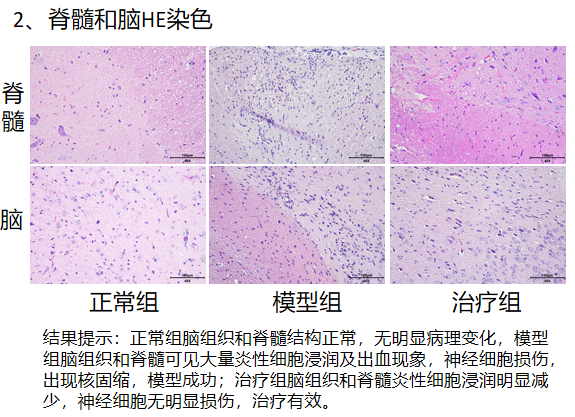
造模:模型组大鼠(Lewis,雌性,6-8周龄)双后肢足掌皮下多点注射原免疫混合液(MBP68-86用PBS溶解后与弗氏完全佐剂1:1体积混合,制成乳剂),从而诱导大鼠产生脑脊髓炎,正常组大鼠则注射等量的生理盐水,造模15天左右。注射后每天对大鼠病变程度评分,造模结束后取脊髓和大脑做HE染色。
阳性药物:芬戈莫德。
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
如想了解实验详情欢迎咨询:
💬 微信公众号「中洪药效评价」咨询
📞 拨打15180153675(微信同号)
🔗 官网https://www.zhbyind.com/
