死亡风险降60%!胰腺癌新药III期碾压化疗,生存期翻倍
2026年4月13日,Revolution Medicines正式官宣,其耗时多年、豪掷20亿美元押注的核心管线药物Daraxonrasib(研发代号RMC-6236),针对转移性胰腺导管腺癌(PDAC)的关键III期临床试验RASolute 302,中期分析圆满达成全部主要终点,拿下注册性临床成功。

来源:Revolution Medicines
说胰腺癌是实体瘤里的“天花板级难题”,真不是夸张:
早期完全没症状,等出现腹痛、黄疸、体重骤降这些信号时,80%以上的患者已经是晚期,连手术根治的机会都没有;还特别“顽固”:90%以上的胰腺导管腺癌都携带RAS突变,偏偏以前的靶向药都是“偏科选手”,只能对付某一种突变,根本覆盖不了大多数患者;油盐不进,耐药性拉满:化疗、免疫药基本打不动它,现有疗法的效果天花板极低;预后惨绝人寰:转移性PDAC患者5年生存率仅3%,二线化疗的中位生存期常年不足7个月,基本上确诊晚期后,大概率只能撑半年多。
而且胰腺癌研发堪称“药企黑洞”——过去12项胰腺癌III期临床试验,超三分之二都失败翻车,研发们啃了几十年硬骨头。
这款新药能打破僵局,核心就是它解决了过去的“致命短板”——以前的RAS抑制剂都是“单打独斗”,只能针对某一种突变;而Daraxonrasib是“全能选手”,能搞定绝大多数RAS突变。
Daraxonrasib是Revolution Medicines自研的口服非共价、激活态(ON-state)泛RAS多亚型抑制剂,和传统RAS抑制剂相比,有两个关键突破:
1. 靶点作用原理升级:传统KRAS抑制剂(如G12C、G12D单靶点药),只能结合单一突变体的闭合构象,而且仅能抑制静息态RAS,对持续激活的癌性RAS作用有限;而Daraxonrasib直接结合激活态RAS(GTP结合型RAS),能阻断RAS与RAF、PI3K等下游效应器的结合,全面抑制RAS-MAPK/PI3K全信号轴,相当于直接掐断癌细胞的“生存命脉”。
2. 突变覆盖谱极广:它能同时覆盖KRAS G12C/G12D/G12V、NRAS、HRAS及野生型RAS,是目前临床进展最快、III期确证有效的“真正泛RAS抑制剂”。而胰腺癌90%以上都是RAS突变,这款药的靶点适配度堪称“量身定制”,完美解决了过去单亚型药物无法覆盖主流患者的痛点。
以前的靶向药是“精准打击但范围窄”,只能对付一小部分患者;而Daraxonrasib是“全面围剿”,不管胰腺癌患者是哪种RAS突变,基本都能覆盖到,而且口服就能吃,不用住院输液遭罪,长期用药也更方便。
FDA方面——突破性疗法认定(BTD)、孤儿药资格、优先审查代金券三重buff叠满,上市审批通道大幅提速,估计不用等太久就能落地临床。
一款药好不好,最终要看临床试验数据——Daraxonrasib的III期结果,刷新纪录,有点离谱的。
这次的RASolute 302试验,是全球多中心、随机对照的III期研究,一共入组了460位“一线化疗已经没用了”的晚期转移胰腺癌患者,一边吃Daraxonrasib,一边用医生常规的标准化疗方案:
新药组中位总生存期(OS):13.2个月;标准化疗对照组中位OS:6.7个月。简单说,吃新药的患者,生存期近乎直接翻倍!更关键的是,死亡风险直接降低了60%,相当于每10个患者里,就有6个人能多争取到更长的生存时间。
除此之外,不管是哪种RAS G12突变的患者,都能明显获益;而且药物安全性特别稳,没有出现未知的副作用,耐受性比化疗好太多——不用遭化疗掉发、恶心、呕吐的罪,口服给药也更方便,长期用药的可行性拉满。
这次的核心数据有两个“历史性突破”:
1. 生存获益幅度刷新纪录:HR=0.40(风险比),意味着全人群死亡风险相对降低60%,在胰腺癌二线及后线治疗领域,这个OS获益幅度是近十年的顶级突破,远超过往所有靶向、免疫联合方案。过去二线化疗的中位OS长期徘徊在6~7个月,而Daraxonrasib直接将这个数字提升到13.2个月,相当于给晚期患者多了一倍的生存希望。
2. 验证了泛RAS抑制策略的可行性:这是全球首个在胰腺癌III期随机对照研究中拿下阳性结果的泛RAS靶向药,彻底验证“激活态RAS抑制”这一技术路线的有效性。
Daraxonrasib的III期成功,整个肿瘤领域不管是临床、行业还是资本市场,都被它狠狠带动。
消息出来的时候Revolution Medicines美股单日暴涨39%,盘中创下历史新高,市值逼近257亿美元;华尔街各大顶级投行紧急上调目标价,美国银行(BofA)、Stifel统一上调至170美元,多家机构给出“强买”评级。
未来上市后,预计将成为首个口服靶向二线标准治疗方案,填补临床空白。同时,它可能还直接带动全球KRAS/RAS抑制剂赛道全线走强,国内相关管线企业也同步迎来估值提振,刺激更多药企投入到泛RAS药物的研发中。
2025年6月,该公司就完成了20亿美元的战略融资,全部用于Daraxonrasib的全球临床开发、商业化布局与全适应症拓展。目前,该药已同步推进4项全球注册III期临床试验,覆盖胰腺癌全病程与肺癌适应症:除了本次成功的二线转移性PDAC(RASolute 302),还有一线转移性PDAC(RASolute 303)、PDAC术后辅助治疗(RASolute 304),以及二线非小细胞肺癌(RASolute 301),未来有望。
虽然Daraxonrasib带来了历史性突破,但我们也得理性看待它的局限性,毕竟没有完美的药物:
1. 目前仅确证二线单药获益:一线治疗、术后辅助治疗的临床数据还未公布,未来能否替代化疗、或与化疗联合进入前线治疗、围手术期治疗,仍需要更多数据验证;
2. 耐药机制尚未明确:长期使用泛RAS抑制剂,癌细胞大概率会出现旁路激活、代偿突变等耐药情况,未来需要布局联合用药方案,进一步延长患者生存期;
3. 人群边界待细化:野生型RAS、携带TP53/CDKN2A等共突变的患者,获益程度还需要等待ASCO 2026年公布的完整数据,进行分层分析才能明确;
4. 国内可及性问题:原研药短期难以快速进入国内市场,后续可能会催生国内药企的me-too/me-better泛RAS管线、授权引进等布局,让国内患者早日用上这款药。
长久以来,胰腺癌因超高的RAS突变率却无对应靶向药,成为肿瘤领域的百年难题。Daraxonrasib的III期临床成功,不仅是Revolution Medicines20亿美元长线押注的胜利,更是泛RAS靶向时代正式降临的标志。实打实的数据证明,60%的死亡风险降低、近乎翻倍的生存期,让晚期患者有看到生的希望。
接下来,我们静待ASCO 2026年完整数据的披露,期待该药尽快向FDA滚动提交上市申请,借助优先审查通道加速落地。也盼着这款重磅新药能早日进入国内,同时带动更多泛RAS药物的研发。
中洪博元——胰腺癌模型
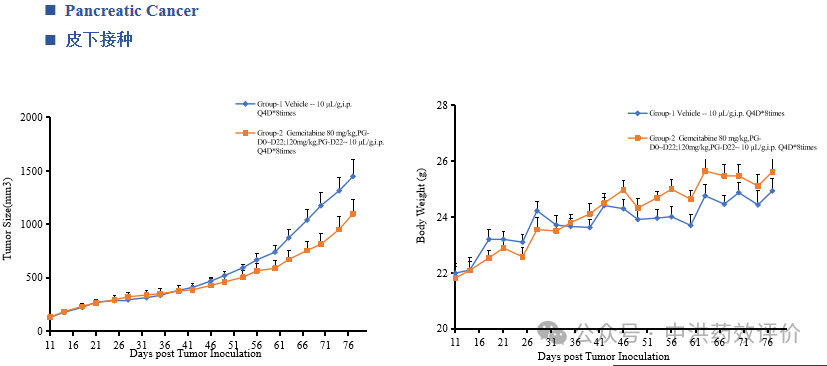
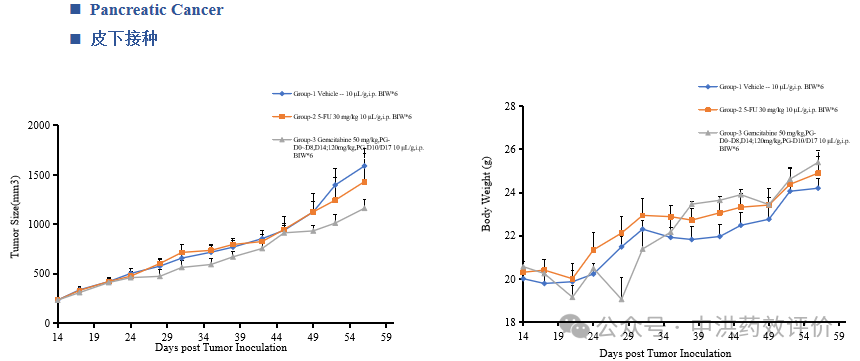
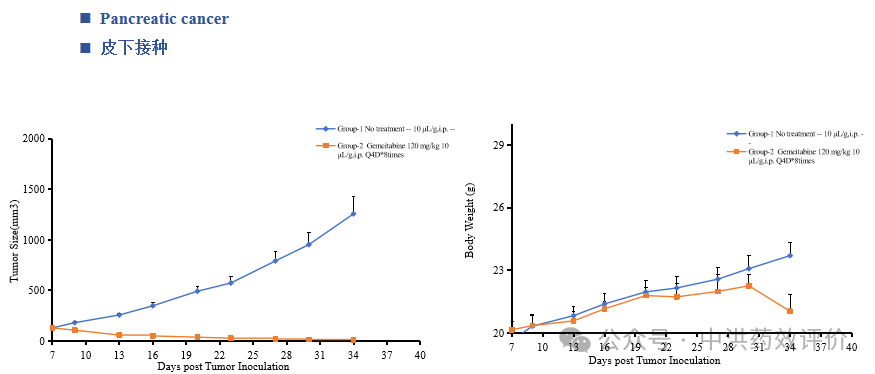
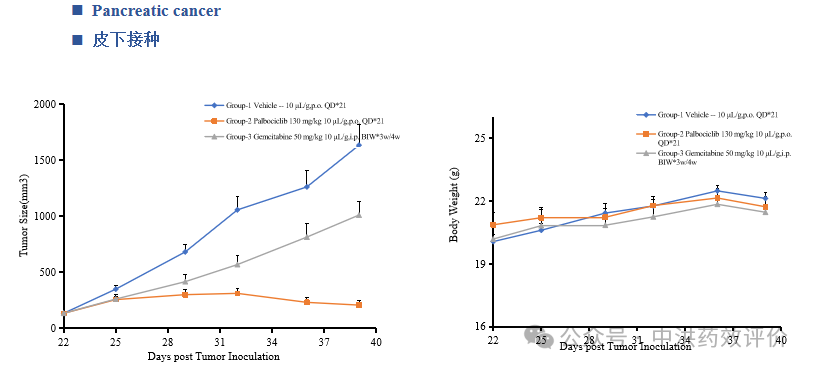
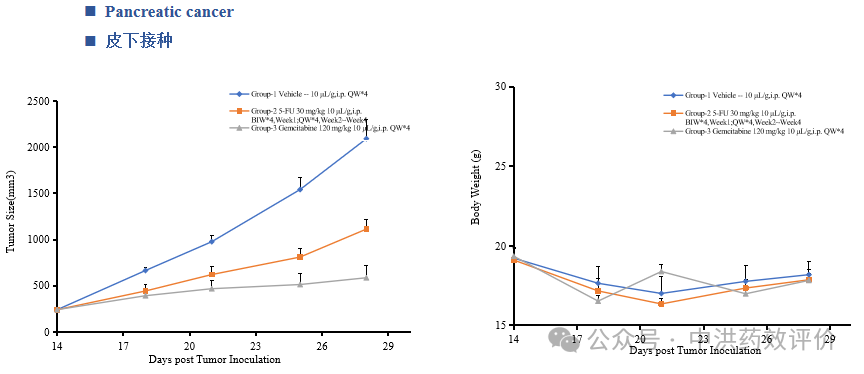
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。