突破衰老密码:2025-2026 衰老机制与干预药物最新进展
衰老是生物体不可避免的生物学过程,但并非单纯的时间流逝,而是由表观遗传紊乱、细胞衰老累积、线粒体功能衰退、慢性炎症等多因素驱动的系统性退行性过程。随着全球老龄化问题日益严峻,衰老的细胞分子机制研究已成为医学生物领域的研究热点。
近年,《Nature》、《Cell》等顶刊发表多项突破性成果,揭示衰老核心机制;国内外药企加速布局靶向衰老通路、细胞清除、基因重编程等创新管线,推动衰老干预从 “延缓” 迈向 “逆转”。本文系统梳理 2025-2026 年衰老领域的机制突破、靶点发现与临床转化进展。
一、衰老机制新认知:从 “线性衰退” 到 “多系统网络崩溃”
传统观点认为衰老是渐进、均匀的过程,而最新研究证实:衰老存在关键转折点、多器官级联调控、细胞与分子网络崩溃,为精准干预提供了全新理论框架。
(一)衰老的 “断崖式” 节点:50 岁与 63 岁
2026 年 3 月,浙江大学、复旦大学联合卡罗林斯卡医学院在《Cell Metabolism》发表重磅研究,分析 50506 名成年人血浆蛋白质组数据,首次证实人体衰老存在两个断崖式关键节点:50 岁与 63 岁。
50 岁:代谢系统、血管系统率先衰退,与衰弱相关蛋白表达剧烈波动,身体从 “缓慢老化” 转入 “加速衰退”。
63 岁:免疫防线崩塌,慢性炎症全面爆发,进入 “炎症型衰弱” 阶段,感染、肿瘤、心血管病风险激增。
这一发现颠覆了 “衰老匀速” 的传统认知,明确50 岁前是衰老干预的黄金窗口期。
(二)血管:衰老的 “先锋枢纽”
2025 年 7 月,中科院刘光慧团队在《Cell》发表研究,构建人类 50 年生命周期蛋白质组衰老图谱,首次证实血管是衰老的 “先锋组织”。血管系统在生命早期即偏离稳态,通过分泌GAS6等促衰蛋白,激活跨器官级联信号,驱动全身多器官系统性衰老。
机制上,血管内皮细胞衰老导致血管通透性增加、微循环紊乱、营养供应不足,进一步加剧组织损伤与衰老。这一发现确立了血管靶向抗衰的核心地位。
(三)线粒体:衰老的 “分子时钟”
2025 年 5 月,中科院李昕团队在《Cell》发表研究,绘制人体组织特异性线粒体突变图谱,揭示线粒体突变累积的“双相时钟” 规律 :
增殖组织(皮肤、肠道):线粒体突变随机扩散,加速衰老与肿瘤风险。
终末分化组织(心脏、大脑):突变集中于特定热点(如 D-loop 区),与能量需求高度相关。
线粒体功能衰退导致ATP 生成减少、活性氧(ROS)堆积、DNA 损伤,是衰老的核心驱动因素。
(四)炎性衰老:慢性炎症是衰老的 “核心引擎”
2025 年中国科学十大进展揭示:慢性炎症是多器官衰老的核心引擎。衰老细胞分泌SASP(衰老相关分泌表型),释放大量促炎因子(IL-6、TNF-α),形成 “炎症 - 衰老 - 炎症” 的恶性循环。
中科院团队发现内源抗衰分子甜菜碱,可精准抑制促炎激酶 TBK1,模拟运动的抗炎、抗衰效果,显著改善老年代谢、肾功能与认知功能。
二、核心靶点突破:从单一通路到多维度干预
基于机制突破,衰老干预已形成mTOR、细胞衰老清除(Senolytics)、NAD+、线粒体、基因重编程五大核心靶点,为药物研发提供明确方向。
(一)mTOR 通路:衰老的 “总开关”
mTOR(哺乳动物雷帕霉素靶蛋白)是调控细胞生长、自噬、代谢的核心通路,抑制 mTOR 可激活自噬、清除损伤细胞器、延缓衰老。
雷帕霉素:经典 mTOR 抑制剂,动物实验可延长寿命 30% 以上。2026 年 3 月,美国启动726 人、3800 万美元大型人体试验,验证雷帕霉素延缓衰老的临床效果。
赛诺根 SRN-901:多通路衰老抑制剂,2024 年临床前数据显示:中年给药使哺乳动物剩余寿命延长33.02%,老年体能从 20% 提升至 50%,肿瘤发生率降低一半。
(二)Senolytics:精准清除衰老细胞
衰老细胞随年龄累积,分泌 SASP 引发炎症与组织损伤,清除衰老细胞是逆转衰老的核心策略。
D+Q 组合:达沙替尼 + 槲皮素,经典 Senolytics,可选择性清除衰老脂肪细胞、内皮细胞。
非瑟酮:天然 Senolytics,清除衰老细胞活性达68%,优于槲皮素、白藜芦醇。
BCL-2 抑制剂:Navitoclax(ABT-263),可清除衰老造血干细胞、肌肉干细胞,改善造血系统早衰。
(三)NAD + 通路:细胞能量与修复的核心
NAD+(烟酰胺腺嘌呤二核苷酸)是能量代谢、DNA 修复、细胞衰老调控的关键分子,随年龄显著下降。
NMN、NR:NAD + 前体,可提升 NAD + 水平,改善代谢、认知、心血管功能。
α-Klotho:长寿基因,2025 年 6 月,Klotho Neurosciences 通过 AAV 基因疗法激活 α-Klotho,小鼠寿命延长20%,显著减缓多器官衰老。
(四)丙酮酸脱氢酶:衰老细胞的 “生存必需靶点”
2026 年 3 月,哈医大周春水团队在《Aging Cell》发表研究,首次证实丙酮酸脱氢酶(PDHA)是衰老细胞的强力靶点。抑制 PDHA 可选择性杀伤衰老细胞,与 Hsp90 抑制剂联合使用,杀伤效率提升50%,显著改善衰老小鼠身体机能。
三、临床转化:从实验室到人体试验的里程碑
2025-2026 年,衰老干预药物加速进入临床,基因疗法、细胞疗法、小分子药物三大方向实现突破性进展。
(一)基因重编程:人体逆龄试验启动
2026 年 3 月,哈佛辛克莱团队ER-100基因疗法正式启动人体临床试验,成为全球首个细胞重编程抗衰人体试验。
机制:AAV 载体导入 OSK(Oct4、Sox2、Klf4)基因,激活细胞年轻化;设计多西环素开关,安全可控。
适应症:青光眼、NAION(致盲眼病),为全身抗衰奠定基础。
(二)干细胞疗法:多器官衰老逆转
2025 年 7 月,中科院刘光慧团队在《Cell》发表研究,工程化抗衰间充质祖细胞(SRC) 输注老年食蟹猴(60-70 岁)44 周:
神经元年轻6-7 岁,认知、记忆提升。
卵母细胞逆转近5 岁,骨密度、血管弹性改善。
衰老细胞减少、基因组稳定性增强。
2026 年 3 月,LongeveronLaromestrocel干细胞药物临床数据显示:9 个月后,衰弱症患者运动耐力提升63.4 米,机体功能 “年轻化”20%。
(三)国产创新药:全球竞争格局突破
瑞初医药 RC017:2026 年 3 月获 FDA 临床批准,中国首个获 FDA 临床的抗衰老创新药,靶向衰老本身,多维度调控衰老细胞。
迈威生物 9MW3811:抗 IL-11 抗体,2025 年与 Calico(谷歌抗衰公司)达成许可,IL-11 敲除小鼠寿命延长 22.5%-25%。
Retro Biosciences RTR242:2025 年 12 月完成首个人体给药,全球首个长寿 1 期临床,修复细胞自噬系统,目标延长健康寿命10 年。
四、国内药企管线布局:从跟跑到领跑
国内药企加速布局衰老干预,覆盖小分子、生物制剂、基因疗法、细胞疗法,形成全球竞争力。
药企 | 药物名称 | 靶点 / 类型 | 研发阶段 | 核心亮点 |
赛诺根(国药合资) | SRN-901 | 多通路衰老抑制剂 | 临床前 | 延寿 33.02%,体能提升 50% |
瑞初医药 | RC017 | 衰老多靶点 | FDA 临床批准 | 中国首个 FDA 临床抗衰药 |
迈威生物 | 9MW3811 | 抗 IL-11 抗体 | I 期完成 | 寿命延长 22.5%-25% |
中科院动物所 | SRC 干细胞 | 抗衰间充质祖细胞 | 临床前 | 灵长类多器官年轻化 |
哈医大 | PDHA 抑制剂 | 丙酮酸脱氢酶 | 临床前 | 选择性清除衰老细胞 |
五、未来展望:精准抗衰与个体化干预
2025-2026 年,衰老研究已从 “延缓” 迈向 “逆转”,未来将呈现三大趋势:
机制深化:解析表观遗传重编程、神经 - 免疫 - 代谢网络,挖掘更多特异性靶点。
精准干预:基于表观遗传时钟、蛋白质组图谱实现精准分型,针对 50 岁、63 岁关键节点制定干预方案。
联合治疗:Senolytics + 自噬激活 + 线粒体修复多靶点协同,实现 “快速控衰 + 长期逆转”。
随着技术突破与临床转化加速,衰老干预将从 “小众前沿” 走向 “全民健康”,大幅降低衰老相关疾病负担,延长人类健康寿命。
动物模型在衰老研究中发挥着不可替代的作用。常用于衰老研究的模式动物有线虫、果蝇、小鼠、大鼠、鼹鼠和恒河猴等。
基于实验成本和实验周期考虑,小鼠是使用范围最广的实验模式动物。在正常生理和饲养条件下,小鼠在18月龄时具有衰老表型,实验周期长且费用高,科学家已通过多种措施建立小鼠早衰模型来缩减实验进程。
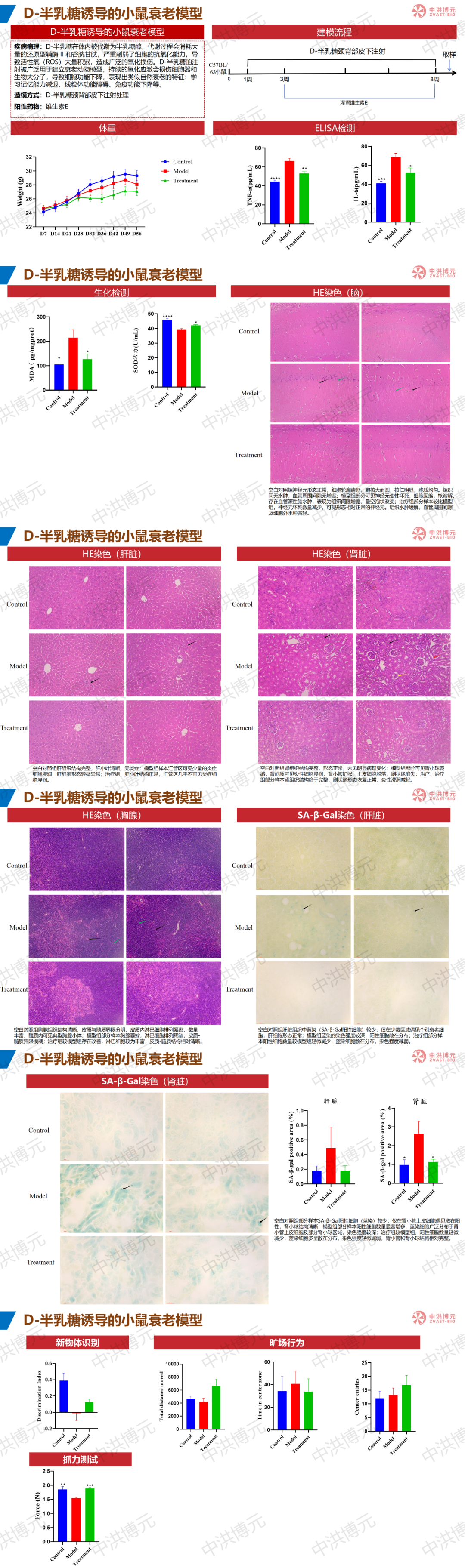
中洪博元——D-半乳糖诱导的小鼠衰老模型
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
