慢性荨麻疹“根治”时代将启? 口服BTK抑制剂或成最终答案
导读:2025年11月诺华新型口服药物Rhapsido(Remibrutinib,瑞米布替尼片)获批上市资格,成为全球首个慢性自发性荨麻疹(CSU)口服BTK抑制剂,从源头阻止肥大细胞和嗜碱性粒细胞释放组胺等致痒介质,为治疗提供新选择。药物临床前测试,中洪博元可提供强大动物模型支持。
诱因难确定,根治难度大
慢性荨麻疹(Chronic Urticaria, CU),是荨麻疹(Urticaria)常见表现种类之一,是一种常见的皮肤黏膜过敏性疾病,其特征表现为皮肤、黏膜小血管暂时性扩张及渗透性增加,导致局部出现大小不等的风团,通常伴有剧烈瘙痒且发作反复。可进一步分为慢性自发性荨麻疹(CSU)和慢性诱导性荨麻疹(CIndU)。截止2025年,中国荨麻疹总患病率为2.6%,其中慢性荨麻疹发病率为1%,超1300万患者饱受病痛困扰。全球约90%慢性荨麻疹患者无法找到明确的外部过敏原。
目前,慢性荨麻疹通常被认为与自身免疫、肥大细胞异常活化、免疫系统功能紊乱等因素密切相关。肥大细胞作为皮肤黏膜的“哨兵”,其胞内储存了大量预合成的组胺等炎症介质, 在慢性自发性荨麻疹中,约30-50%的患者存在自身免疫病因。其体内自发的产生了针对自身IgE或IgE受体(FcεRⅠ)的IgG型自身抗体。这些受体交联“错误”导致布鲁顿酪氨酸激酶(BTK)被磷酸化激活,致使释放组胺分子,自发的引起风团瘙痒,同时合成并释放白三烯、前列腺素、血小板活化因子,以及多种细胞因子(如TNF-α, IL-6)和趋化因子,加剧炎症、浸润,形成慢性、持续的炎症循环。
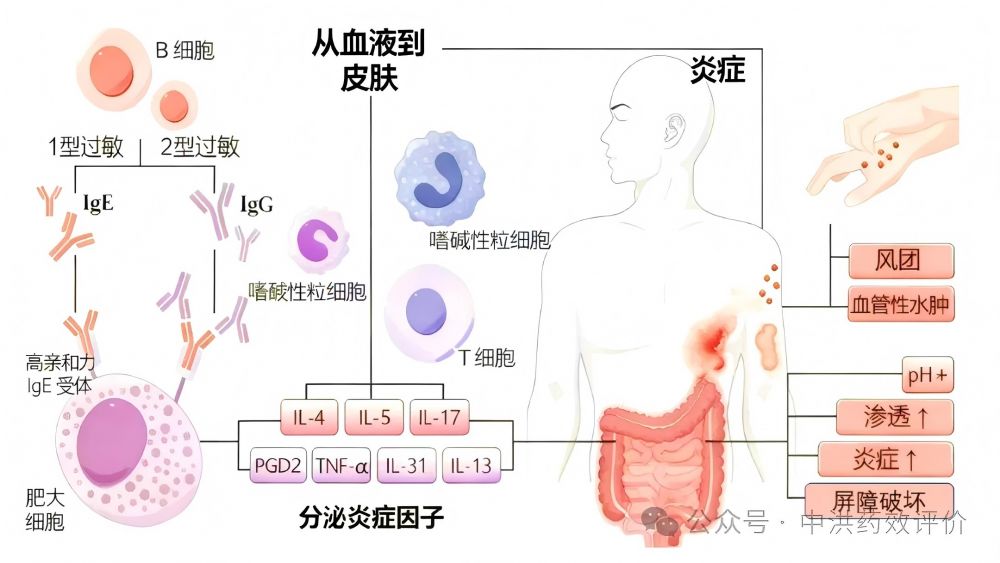
图片来源:药智新闻
破局之匙:从“抗组胺”到“源头抑制”的BTK抑制剂
目前,市面上常见荨麻疹治疗药物是以氯雷他定、左西替利嗪、卢帕他定为代表的二代H1抗组胺药物,通过竞争性阻断组胺与H1受体结合,减轻血管扩张及瘙痒,仅是控制已发生的症状。情形严重时,可加用以奥马珠单抗为代表的抗IgE单克隆抗体药物,作用于已经形成的游离IgE。但这均未靶向于致敏因子的源头布鲁顿酪氨酸激酶(BTK),导致约60%患者标准剂量控制不佳,增量后仍有大量患者无效。
2025年11月,诺华公司宣布其创新口服药物Rhapsido(Remibrutinib,瑞米布替尼片) 正式获得中国国家药品监督管理局及FDA批准,用于治疗抗组胺药控制不佳的成人CSU患者。成为当今全球首个获批用于CSU的口服布鲁顿酪氨酸激酶抑制剂(BTKi)。
诺华发布的临床数据显示,对于二代H1抗组胺药治疗后仍有症状的患者,瑞米布替尼在治疗早期即显著改善症状,且疗效持续至第52周。与第12周结果一致,瑞米布替尼在24周时相显示出显著优势。第2周及第12周,瑞米布替尼组达到疾病良好控制(UAS7≤6)的患者比例显著高于安慰剂组,其中约三分之一患者在12周时瘙痒和风团完全消失。第24周时,原安慰剂组患者转而接受瑞米布替尼治疗,疗效在转换第一周内即可显现,并持续至研究结束(共治疗28周)。至第52周,近半数患者实现无瘙痒、无荨麻疹症状(UAS7=0)
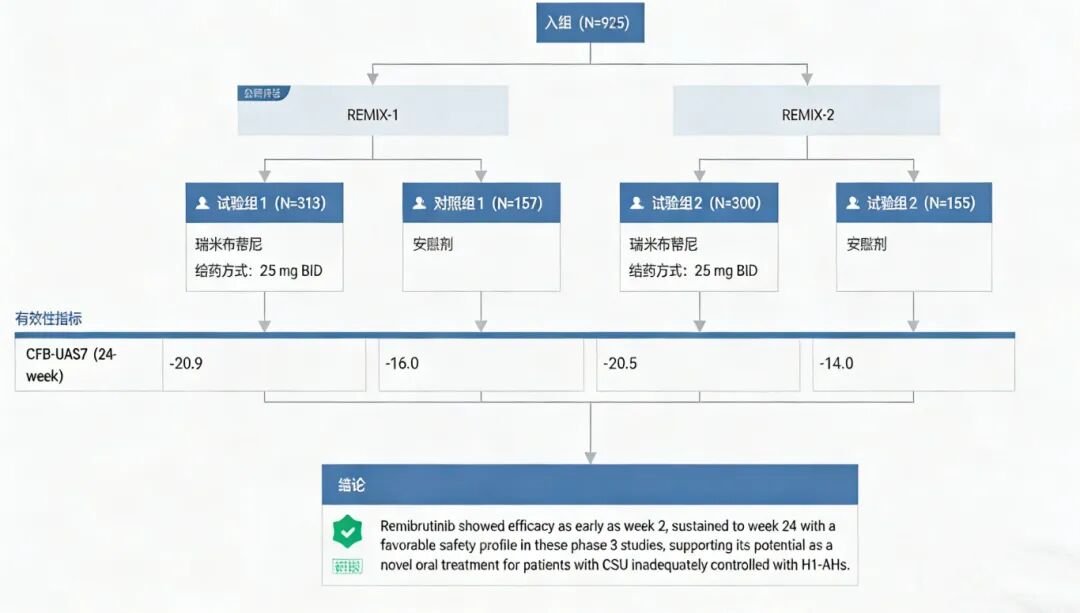
图片来源:Insight 数据库网页版
瑞米布替尼通过不可逆的共价键与非活性构象的BTK结合发挥作用,该药在难治性CSU患者中表现出显著的疗效和良好的安全性,目前,该药在欧盟、日本和中国均处于上市申请审评阶段,且该产品在中国已经被NMPA纳入优先审评。为难治性CSU另一重要治疗选择。
中洪博元,可为“过敏动物模型”提供支持
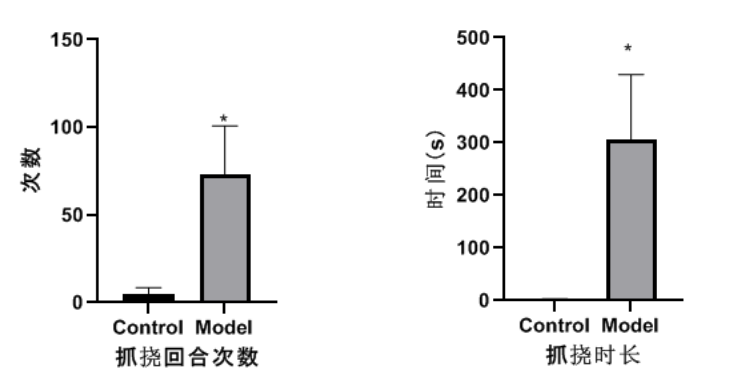
一、慢性瘙痒--C48/80诱导小鼠皮肤过敏模型数据
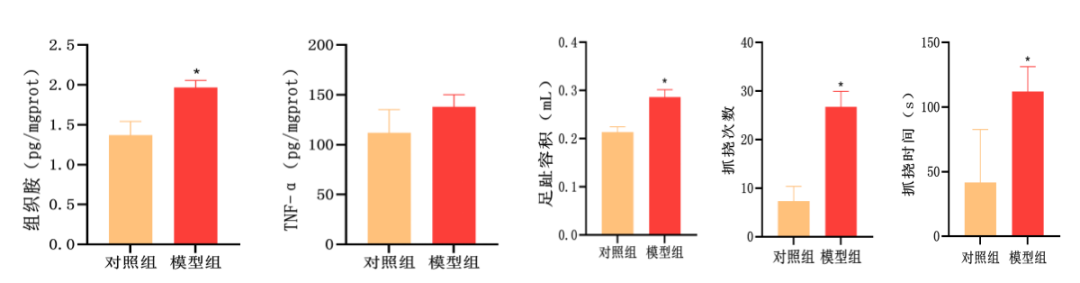
二、急性瘙痒---P物质诱导小鼠皮肤瘙痒模型
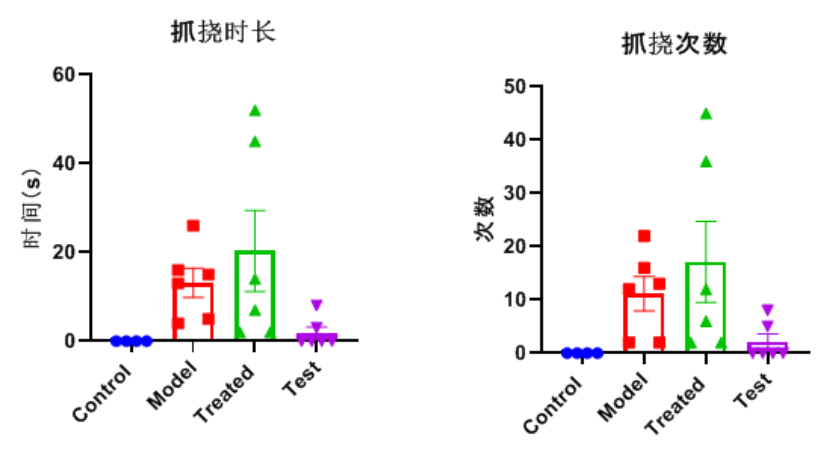
三、急性瘙痒---化合物C48/80诱导小鼠皮肤瘙痒模型
四、急性瘙痒---氯喹诱导小鼠皮肤瘙痒模型
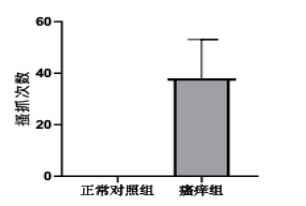
五、急性瘙痒---胆红素诱导小鼠皮肤瘙痒模型
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
