CRC治疗新拐点:INHBA致癌双重路径破解,5 款新药抢滩
结直肠癌(Colorectal cancer,CRC)是一种常见的恶性肿瘤,其发病机制尚未完全阐明。肿瘤微环境(tumor microenvironment, TME)和铁死亡是肿瘤进展和转移的关键驱动因素。近期,湘雅医学院“90后”博士团队在顶级期刊揭示全新结直肠癌(CRC)致癌机制,此外,多款靶向、免疫创新药获批或取得关键进展。
图源:中洪博元
科研前沿:双重机制锁定INHBA,提供新靶点
2025年12月26日,师从魏于全教授的中南大学湘雅医学院“90后”博士相关团队(袁霞、周艳宏等)在Signal Transduction and Targeted Therapy(IF=52.7)发表题为“Inhibin beta A drives colorectal cancer progression through macrophage M2 polarization and mitochondria-dependent ferroptosis suppression”的研究论文,首次系统阐明INHBA(抑制素βA)驱动结直肠癌进展的双重分子机制。
该研究首先通过TCGA、GEO等公共数据库挖掘,发现INHBA在结直肠癌组织中显著高表达,且与患者总生存期(OS)、无病生存期(DFS)缩短直接相关,多因素Cox回归分析进一步确认其为独立预后风险因子。
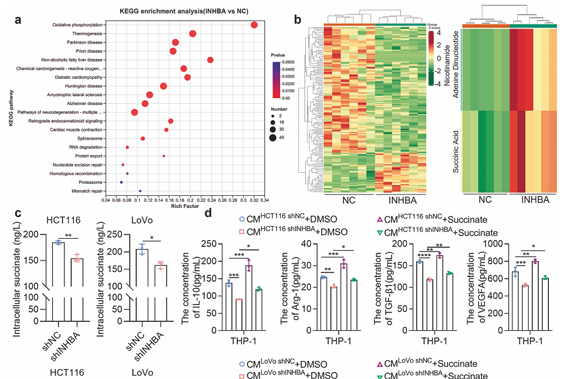
图源:Signal Transduction and Targeted Therapy
其次,在动物模型中完成功能验证:INHBA过表达可显著促进移植瘤生长,而敲低INHBA则能有效抑制肿瘤增殖与侵袭。这一设计排除靶点与肿瘤进展的相关性干扰,明确INHBA的核心驱动地位。
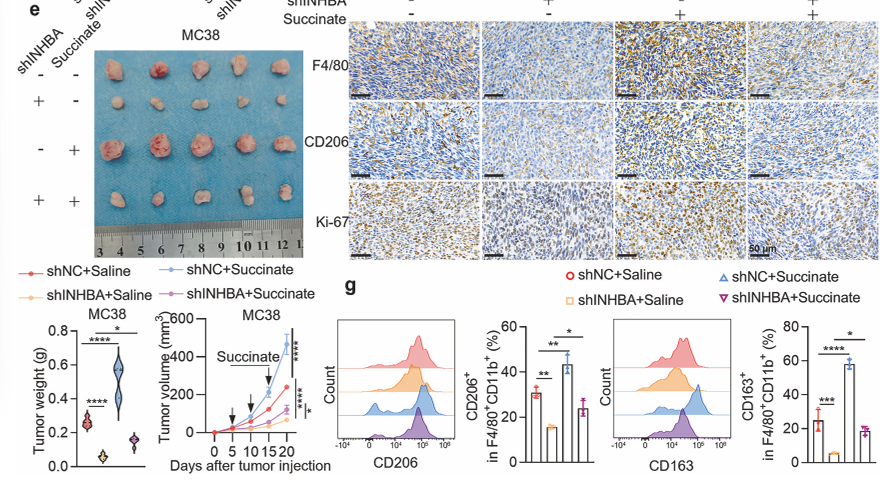
图源:Signal Transduction and Targeted Therapy
最关键的是研究发现INHBA通过两条独立路径协同推动肿瘤进展(“免疫微环境重编程+铁死亡抑制”的双重机制)。一方面,INHBA上调线粒体蛋白SLC25A10,激活琥珀酸/SUCNR1轴驱动肿瘤相关巨噬细胞(TAMs)向M2表型极化,同时作为支架蛋白抑制E3泛素连接酶TRIM21介导的SLC25A10降解,稳定该蛋白以强化免疫抑制微环境;另一方面,通过mtGSH/GPX4轴抑制线粒体依赖性铁死亡,维持癌细胞存活。提示我们靶向INHBA-SLC25A10-琥珀酸轴,或联合免疫检查点抑制剂与铁死亡诱导剂,有望为晚期结直肠癌患者提供更精准的治疗。
产业转化破解临床痛点
这些获批或进展中的项目均精准瞄准临床未满足需求,其研发思路各有侧重,既是对疾病分型的深度把握,也展现了不同靶点领域的技术突破方向。
齐鲁制药安可泽®:齐鲁制药帕妥尤单抗N01注射液(安可泽®)作为国内首个全人源抗EGFR单抗,2025年12月9日获批,12月21日正式供药。研发核心思路是通过全人源化设计提升药物安全性。Ⅲ期研究显示,其联合FOLFOX方案用于RAS野生型转移性结直肠癌一线治疗,中位PFS达11.2个月,显著优于对照组的8.3个月(HR=0.61),输液反应发生率仅1.2%,且均为1-2级,安全性显著优于传统药物。安可泽®的商业化落地有望打破进口抗EGFR单抗的垄断局面,凭借“疗效相当、安全性更优”的核心竞争力抢占RAS野生型结直肠癌一线治疗市场。

图源:国家药品监督管理局官网
加科思JAB-23E73:2025年12月22日,加科思与阿斯利康就泛KRAS抑制剂JAB-23E73达成全球独家许可协议,拟将该药物拓展至结直肠癌等KRAS突变实体瘤领域。KRAS曾长期被视为“不可成药”靶点,虽近年G12C特异性抑制剂取得突破,但对于G12A、G12V等其他突变亚型仍缺乏有效治疗手段。加科思的研发思路是开发“泛KRAS抑制剂”,覆盖多种KRAS突变体及野生扩增型,实现“一药多突变”的治疗效果。JAB-23E73的核心研发特点在于其既可抑制GDP结合状态(OFF状态)的KRAS向GTP结合状态转化,也可抑制GppNp结合状态(ON状态)的KRAS与cRAF的相互作用,从而强效阻断KRAS下游信号通路。目前其I期临床正在中美同步开展。根据合作协议,加科思将获得1亿美元首付款及最高19.15亿美元的里程碑付款,阿斯利康负责中国以外市场的临床开发、注册及商业化,双方在中国市场共同推进;这种“早期研发+全球商业化”的分工模式,将高效推动泛KRAS抑制剂这一重磅靶点药物的转化进程。
Cartography Bio CBI-1214:2025年12月23日,Cartography Bio的双抗药物CBI-1214获FDA批准IND并授予快速通道资格,用于结直肠癌治疗,其研发思路聚焦于“突破免疫冷肿瘤瓶颈,覆盖微卫星稳定型(MSS)/微卫星不稳定性低(MSI-L)主流亚型”。CBI-1214的研发核心是“精准靶向肿瘤抗原+T细胞定向激活”:作为T细胞结合剂(双特异性抗体),其一端靶向结直肠癌细胞表面高特异性抗原LY6G6D(健康细胞低表达,安全性高),另一端结合T细胞,通过“桥梁作用”将T细胞直接招募至肿瘤细胞旁并激活,实现精准杀伤。LY6G6D在MSS/MSI-L亚型中高表达,精准覆盖免疫治疗不敏感的主流人群;同时通过蛋白工程优化提升抗肿瘤活性,避免传统免疫治疗的脱靶效应。FDA快速通道资格的授予,充分认可了其解决未满足临床需求的潜力,预计2026年Q1启动的I期临床将成为其关键里程碑。
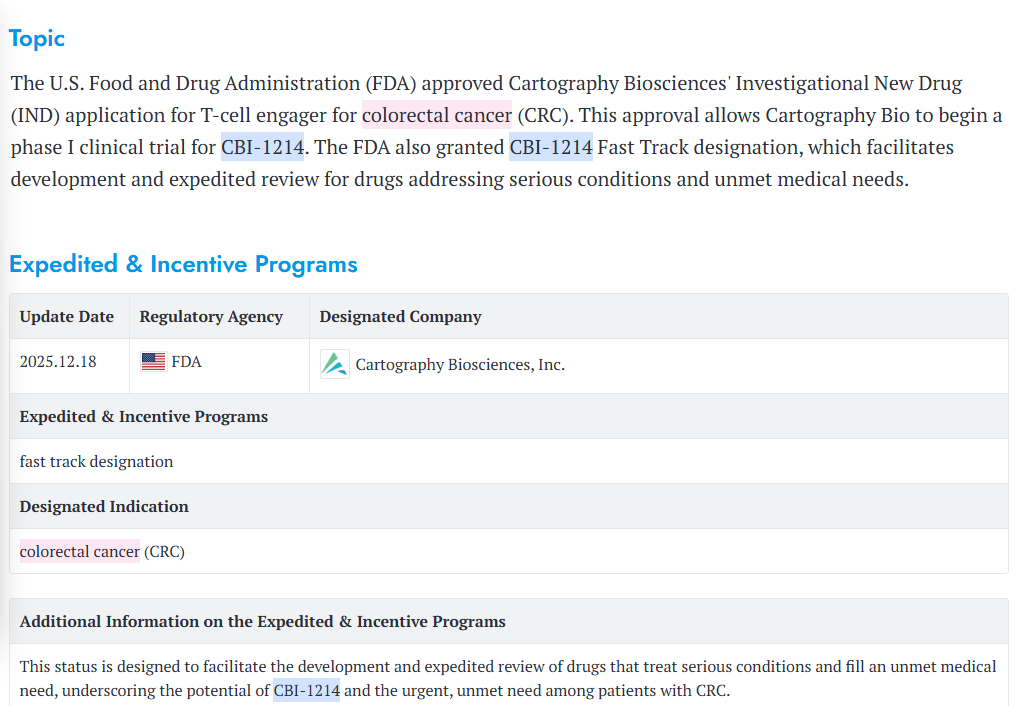
图源:BIO-RESEARCH.AI
信达生物“舒欣CP”:2025年12月25日,信达生物双免疫组合(伊匹木单抗N01+信迪利单抗)获批用于可切除IIB-Ⅲ期MSI-H/dMMR结肠癌新辅助治疗,成为全球首个该场景下的双免疫方案,其研发思路精准抓住“早期患者免疫功能更完整,术前免疫激活可建立长期免疫记忆”的核心。其特点在于“协同增效+安全性平衡”:PD-1单抗(信迪利单抗)可解除T细胞抑制、恢复增殖,直接杀伤肿瘤细胞;CTLA-4单抗(伊匹木单抗N01,国产首个)则能促进T细胞活化、削弱肿瘤免疫逃逸,两者协同强化免疫应答。临床试验数据充分验证了这一思路的有效性:NeoShot-Ⅲ期中首批50例患者中82%达到pCR,且双免方案下手术完全切除率达100%,多数患者可免于术后辅助化疗。
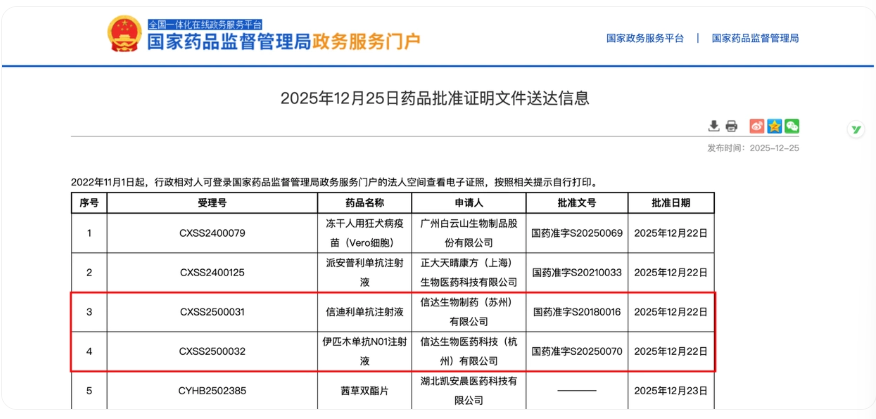
图源:国家药品监督管理局官网
科州药物IPO:2025年12月31日,北交所受理科州药物IPO申请,其核心产品为妥拉美替尼胶囊(商品名:科露平®),这是我国自主研发的首款MEK抑制剂、全球首个且唯一获批针对NRAS突变晚期黑色素瘤适应症的MEK抑制剂,已纳入医保,管线涵盖结直肠癌等肿瘤。科州药物聚焦于“成熟靶点的优化与适应症拓展”,MEK作为MAPK通路的关键节点,与KRAS、BRAF等靶点存在协同作用,妥拉美替尼在结直肠癌中的应用有望通过联合治疗提升疗效。此次IPO将进一步助力其管线推进,强化在肿瘤靶向治疗领域的布局。
湘雅医学院团队的INHBA双重机制研究,为联合治疗提供了全新理论方向;而信达、齐鲁、加科思等企业的研发项目,则分别从免疫组合、全人源靶向、泛突变抑制、双抗导向等不同赛道,精准破解临床痛点。无论是INHBA的双重路径解析,还是KRAS、LY6G6D等靶点的精准选择,均源于对疾病分子机制的深度理解。
中洪博元结肠癌模型介绍
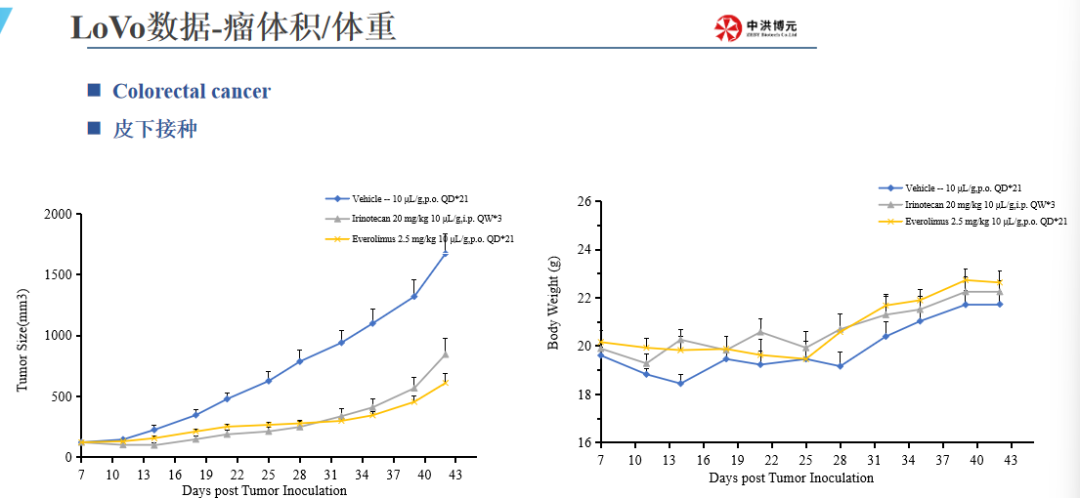
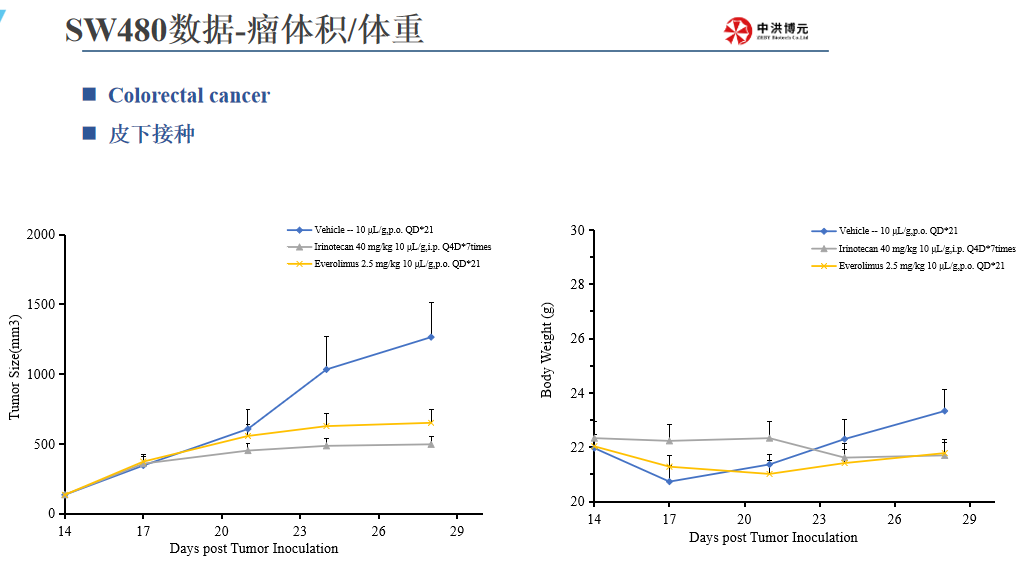
参考文献
Li W, Liang L, Liu S, Tang J, Ou S, Yuan Z, Zhou Y, Yuan X. Inhibin beta A drives colorectal cancer progression through macrophage M2 polarization and mitochondria-dependent ferroptosis suppression. Signal Transduct Target Ther. 2025 Dec 26;10(1):420. doi: 10.1038/s41392-025-02518-y. PMID: 41449244; PMCID: PMC12741050.
