胰腺癌模型 | 攻克 “不可成药” 靶点!胰腺癌新药疗效惊艳
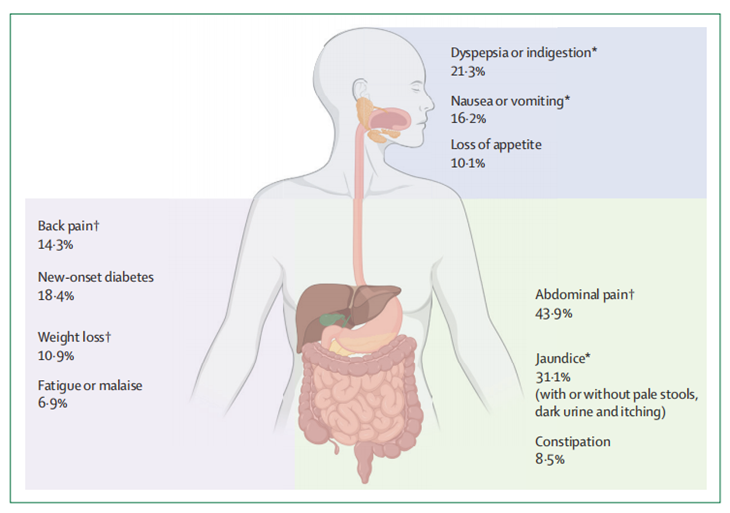
有一种癌,被称为沉默的“杀手”,但早期症状并不明显,以至于被发现时已经是晚期,它就是胰腺癌,胰腺癌的恶性程度高,5年生存率不足10%,远远低于乳腺癌、肺癌,所以很多人称它为“癌王”。
发病率呈持续攀升态势。其最大诊疗痛点在于起病隐匿,早期缺乏特异性症状,导致多数患者确诊时已进展至中晚期,治疗难度极大且预后极差。据《CA: A Cancer Journal for Clinicians》2024 年发布的研究数据,胰腺癌患者五年生存率仅为13%,目前已跃升为全球第六大癌症致死原因。2022年,全球新发胰腺癌病例超51万例,死亡人数达46万例,且有预测显示,该病将在 2040年进一步攀升为全球第二大癌症死因,给全球公共卫生领域带来严峻挑战。
长期以来,晚期胰腺癌治疗以化疗为主,疗效瓶颈显著。2025年以来,随着靶向治疗、免疫治疗及双特异性抗体等技术的突破,胰腺癌新药研发领域迎来多项关键进展,为患者带来全新治疗希望。
图源于网络
一、靶向KRAS突变,突破“不可成药”瓶颈
KRAS突变是胰腺癌最核心的分子驱动因素,超过90%的胰腺导管腺癌(PDAC)患者存在KRAS突变,其中KRAS G12D亚型占比高达40%。此前近40年,KRAS因蛋白结构特性被视为“不可成药”靶点,2025年口服KRAS G12D抑制剂的临床突破成为该领域里程碑。
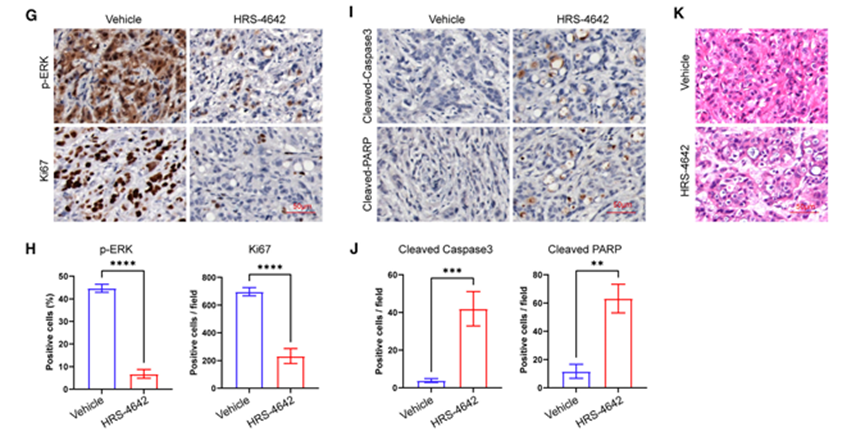
2025年10月,恒瑞医药在2025年ESMO大会上公布了HRS-4642联合吉西他滨与白蛋白紫杉醇治疗KRAS G12D突变型晚期胰腺癌的1b/2期临床数据。HRS-4642是恒瑞医药自主研发的高亲和力、选择性、长时效非共价KRAS G12D抑制剂,也是首个被报道临床有效的KRAS G12D特异性抑制剂。此前,HRS-4642的基础研发成果已发表于国际顶级医学期刊《Cancer Cell》,证实其可特异性结合KRAS G12D,双重阻滞下游信号通路,且倾向于瘤内蓄积,药代动力学与药效学特征优异。不仅为KRAS G12D突变患者提供新选择,更推动非共价结合等创新成药技术的发展。
临床数据显示:中位随访7.5个月后,确认客观缓解率(ORR)达63.3%,超半数患者肿瘤显著缩小,较标准化疗大幅提升;疾病控制率(DCR)高达93.3%,表明绝大多数患者的肿瘤生长得到有效控制,而既往化疗DCR通常不超70%;中位无进展生存期(PFS)尚未成熟,但6个月PFS达89.3%,疾病进展风险显著降低。
图源于Cancer Cell
二、双特异性抗体,破解毒性难题
双特异性抗体通过同时靶向肿瘤细胞表面两个靶点,实现精准杀伤与肿瘤微环境调控,同时降低单靶点药物的毒性风险。2026 年ASCO GI上,Phanes Therapeutics 自研的 spevatamig 公布关键临床数据,以 93% 的疾病控制率和显著延长的生存期,为被称为 “癌王” 的胰腺癌治疗带来突破性希望,突破了传统CD47药物的血液毒性瓶颈。
Spevatamig采用独特的PACbody®和SPECpair®双特异性抗体技术平台设计,其两个抗体单臂分别靶向CLDN18.2和CD47,通过优化抗CD47单臂和单臂靶向设计,有效降低了CD47相关的血液毒性和CLDN18.2相关的胃肠道毒性。
临床数据显示,在2 mg/kg spevatamig每周一次给药联合GnP一线治疗mPDAC的15例患者中(n=15),有6例患者达到部分缓解(其中5例已确认,1例待确认)、8例患者疾病稳定,疾病控制率为93%(对比关键临床研究中的48%),客观缓解率为40%。
目前,spevatamig正处于美国II期与中国II期临床阶段,是全球同靶点药物中,临床进度最快的管线。此前已获FDA胰腺癌孤儿药资格及转移性Claudin18.2阳性胰腺癌快速通道资格。此番公布的TWINPEAK研究阶段性数据,是spevatamig走向临床应用的关键一步。

图源于网络
三、免疫治疗:三联方案突破一线治疗瓶颈
胰腺癌因独特的“免疫荒漠”肿瘤微环境,导致传统PD-1/PD-L1抑制剂单药在转移性胰腺癌(mPDAC)中疗效惨淡,未能达到临床转化的核心标准——无论是帕博利珠单抗、纳武利尤单抗等代表性药物,均无法显著改善患者症状,目前全球尚无任何单药方案获批用于mPDAC的一线、二线及后续治疗。为突破单药疗效瓶颈,临床虽开展了大量传统PD-1/PD-L1抑制剂联合化疗(如吉西他滨+白蛋白紫杉醇)的探索,但多数方案仅能小幅提升疗效,未能实现实质性突破。2025年,PD-1/TGF-β双功能融合蛋白联合方案获批Ⅲ期临床试验,为破解这一长期困局带来了关键突破。
TQB2868由正大天晴自主研发,可同时阻断PD-1/PD-L1通路并中和肿瘤微环境中的TGF-β,兼具免疫检查点抑制与肿瘤微环境重塑双重作用。其联合安罗替尼与AG化疗构建的“免疫-靶向-化疗”三重协同方案,于2025年6月获中国国家药品监督管理局药品审评中心批准开展Ⅲ期注册临床试验。
该联合方案已于2025年ASCO年会首度公布Ⅱ期临床研究结果,显示出令人瞩目的临床获益。在接受TQB2868联合安罗替尼与化疗的mPDAC患者中,客观缓解率(ORR)高达63.9%,疾病控制率(DCR)达100%;中位无进展生存期(PFS)尚未达到,6个月PFS率达86%;中位总生存期(OS)尚未达到,但预期有望首次在此类患者中突破1年大关(该预期基于当前Ⅱ期临床数据趋势,仍需Ⅲ期大样本研究验证)。

图源于ASCO
目前,全球尚无PD-1/TGF-β双功能融合蛋白获批上市,TQB2868研发进度全球排名一。该联合疗法将有望成为免疫检查点抑制剂在胰腺癌的首个一线治疗方案,为胰腺癌患者的总生存期、生活质量带来根本性改善。
总结
2025年以来,胰腺癌新药研发在多个方向实现关键突破:KRAS G12D抑制剂打破“不可成药”壁垒,双特异性抗体破解传统靶点毒性难题,“免疫+靶向+化疗”联合方案有望填补一线免疫治疗空白。这些进展均以精准治疗为核心,通过靶点创新、技术优化和方案协同,显著提升了疗效并改善了安全性。
未来,随着多项Ⅲ期临床试验的推进,有望有更多新药或新方案获批上市,改写胰腺癌治疗格局。同时,个体化治疗(如mRNA疫苗)、多靶点药物研发以及联合治疗策略的优化,将持续成为研发热点,为进一步提升胰腺癌患者生存率、改善生活质量提供更多可能。
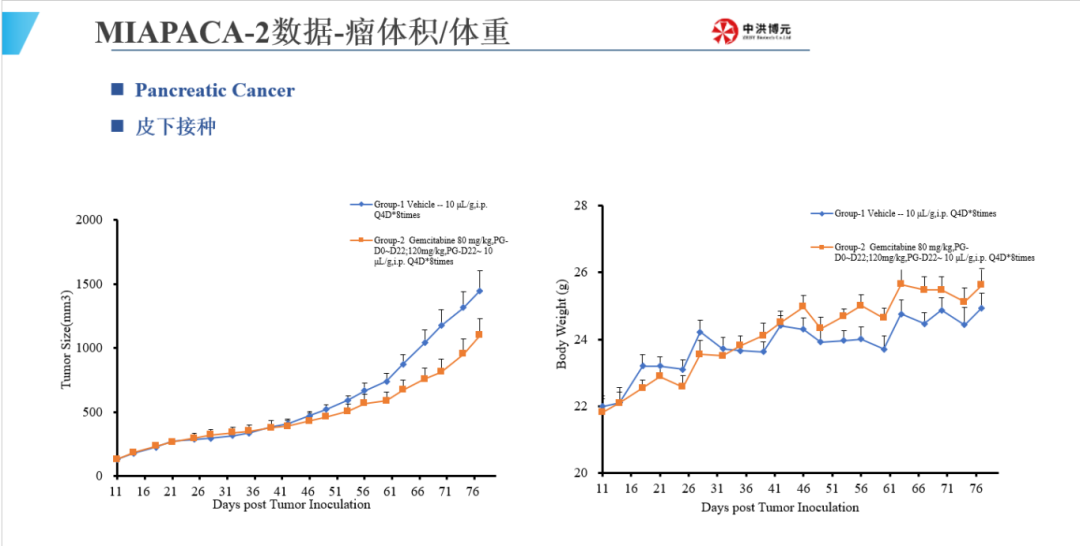
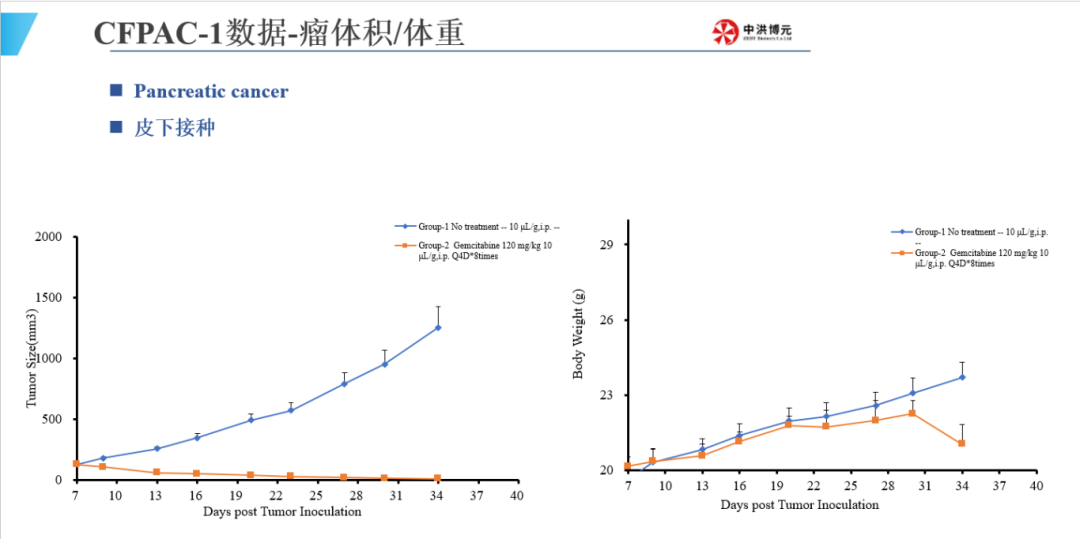
中洪博元胰腺癌模型
参考文献:
(1)Zhou C,etc. Anti-tumor efficacy of HRS-4642 and its potential combination with proteasome inhibition in KRAS G12D-mutant cancer. Cancer Cell. 2024 Jul 8;42(7):1286-1300.e8.
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
