突破免疫紊乱困局:SLE精准治疗最新进展
系统性红斑狼疮(SLE)是一类复杂的自身免疫性疾病,因体内免疫耐受失衡,产生大量致病性自身抗体与免疫复合物,导致皮肤、关节、肾脏等多器官系统受损,好发于育龄期女性,我国患者超百万,疾病负担居全球前列。
传统治疗依赖糖皮质激素、免疫抑制剂等广谱方案,存在缓解率低、复发率高、长期用药毒副作用显著等痛点。
近年,随着单细胞测序、基因编辑与生物制剂技术的飞速发展,SLE 研究在遗传机制、核心靶点与细胞治疗领域取得颠覆性突破,多篇成果发表于 Nature、NEJM 等顶刊,多款新药进入 III 期临床,为患者带来根治曙光。
一、遗传机制新突破:PLD4 基因突变 —— 单基因狼疮致病新靶点
SLE 发病具有高度异质性,遗传因素是核心驱动之一。2025 年 9 月,浙江大学刘志红院士团队在Nature发表重磅研究,首次证实PLD4 基因功能缺失突变可直接导致SLE;阐明了PLD4突变引起Toll样受体7(TLR7)和TLR9过度活化,激活Ⅰ型干扰素信号通路,驱动浆细胞样树突状细胞(pDCs)与浆细胞(PCs)内在性扩增,导致自身免疫稳态失衡和SLE的核心分子机制;提出了基于核心致病通路的精准干预策略。

二、B 细胞通路革新:双靶点生物制剂 —— 泰它西普引领标准治疗升级
B 细胞异常活化是 SLE 发病的核心环节,其存活与分化依赖 BLyS、APRIL 双因子调控。2025 年 10 月,北京协和医院张奉春团队牵头的泰它西普 III 期研究登顶NEJM,确立国产双靶点生物制剂的全球领先地位。
该随机双盲试验纳入 335 例活动性 SLE 患者,结果显示:泰它西普组 52 周 SRI-4 应答率达 67.1%,显著高于安慰剂组 32.7%(P<0.001);疾病活动指数(SELENA-SLEDAI)降幅达 - 4.95,中位复发时间延长至 198 天(安慰剂组 115 天),44.9% 患者实现激素减量(≤7.5mg / 天)。药物同时阻断 BLyS、APRIL,全面抑制 B 细胞成熟与自身抗体生成,安全性优于单靶点生物制剂。
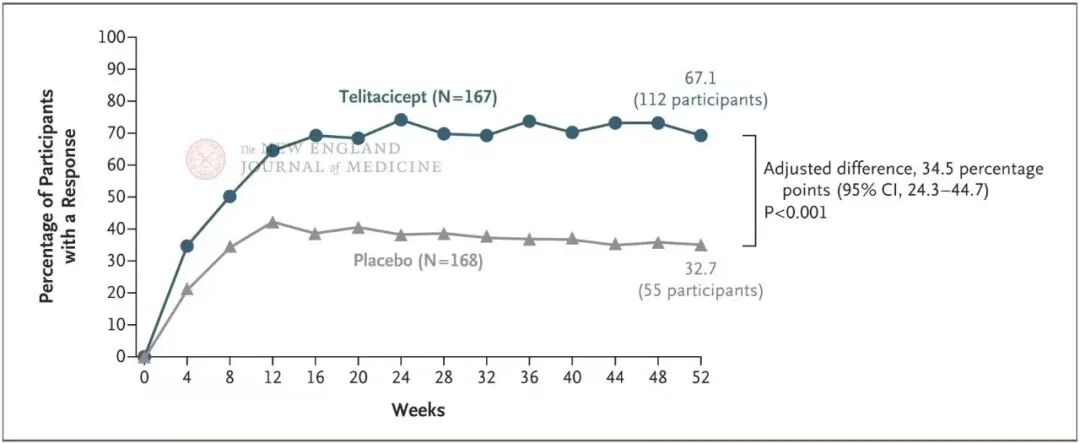
目前泰它西普已在中国获批,III 期扩展研究覆盖全球多中心,有望成为中重度 SLE 一线联合方案,推动 “激素减量、长期缓解” 的治疗目标。
三、新兴靶点崛起:BTK 抑制剂与 I 型干扰素通路 —— 难治性 SLE 新希望
1. BTK 抑制剂:奥布替尼突破 B 细胞活化关键节点
布鲁顿酪氨酸激酶(BTK)调控 B 细胞受体信号,是 SLE 治疗潜力靶点。2025 年 12 月,诺诚健华宣布奥布替尼治疗 SLE 的 IIb 期研究达主要终点,高剂量组应答率超 60%,显著优于安慰剂。
III 期临床已启动,采用每日 75mg 方案,可抑制 B 细胞活化、增殖与抗体分泌,同时降低炎症因子释放,对合并狼疮肾炎、皮肤受累患者疗效突出。作为国产高选择性 BTK 抑制剂,奥布替尼安全性良好,感染风险低于传统免疫抑制剂,有望填补难治性 SLE 治疗空白。
2. I型干扰素通路:Saphnelo(Anifrolumab)重塑亚洲人群证据
I 型干扰素过度激活是 SLE 核心炎症通路。2026 年 2 月,Anifrolumab(抗 IFNAR1 单抗)亚洲 III 期试验(AZALEA)公布积极结果:治疗组 BICLA 缓解率 60.3%、SRI-4 缓解率 65.1%,均为安慰剂组近 2 倍。
药物阻断 I 型干扰素受体,显著改善皮肤、关节症状,60% 以上患者实现激素减量,安全性与全球数据一致。目前已在欧美获批,中国上市申请推进中,为干扰素通路活化的 SLE 患者提供精准选择。
四、细胞治疗革命:CAR-T 与体内基因编辑 —— 迈向 “功能性治愈”
1. 双靶点 CAR-T:清除致病 B 细胞全谱系
2025 年 11 月,上海长征医院黄河团队在Science Translational Medicine发表 CD19/BCMA 双靶点 CAR-T 治疗 SLE 的 I 期结果。
研究纳入 15 例难治性患者,12 周应答率 100%,86.7% 实现完全缓解,抗 dsDNA 抗体转阴、补体恢复正常,中位随访 712 天无复发。疗法同时清除 CD19+B 细胞与 BCMA + 浆细胞,实现免疫 “重置”,安全性优异,无严重细胞因子释放综合征。部分患者实现 3 年无药缓解,开启 “功能性治愈” 新范式。
2. 体内 CAR-T:LNP-mRNA 技术突破传统壁垒
2025 年 9 月,中国科大附一院陈竹团队在NEJM发表全球首个体内 CAR-T治疗 SLE 的研究。
采用靶向 CD8+T 细胞的 LNP-mRNA(HN2301),直接在体内生成 CD19-CAR-T 细胞。5 例难治性患者单次输注后,6 小时即检测到 CAR-T 细胞,B 细胞降至基线 10%,4 例狼疮肾炎患者蛋白尿显著改善,无严重不良事件。该技术无需体外细胞制备,成本降低 90%、周期缩至 1 天,为 SLE 细胞治疗普及化奠定基础。
五、临床转化与未来展望
SLE 研究已形成 “遗传机制 — 核心通路 — 细胞治疗” 的完整创新链:PLD4 等单基因靶点推动精准分型;泰它西普、奥布替尼等新药重构标准治疗;CAR-T 与体内基因编辑直指 “根治” 目标。
未来随着 III 期临床完成与新药获批,SLE 将进入 “精准靶向、长期缓解、低毒安全” 的全新时代。多靶点联合、基因分型指导个体化用药、细胞治疗标准化将成为主流,最终降低器官损伤与死亡率,让 SLE 从 “不死癌症” 变为可控可治的慢性疾病。
SLE模型研究进展:
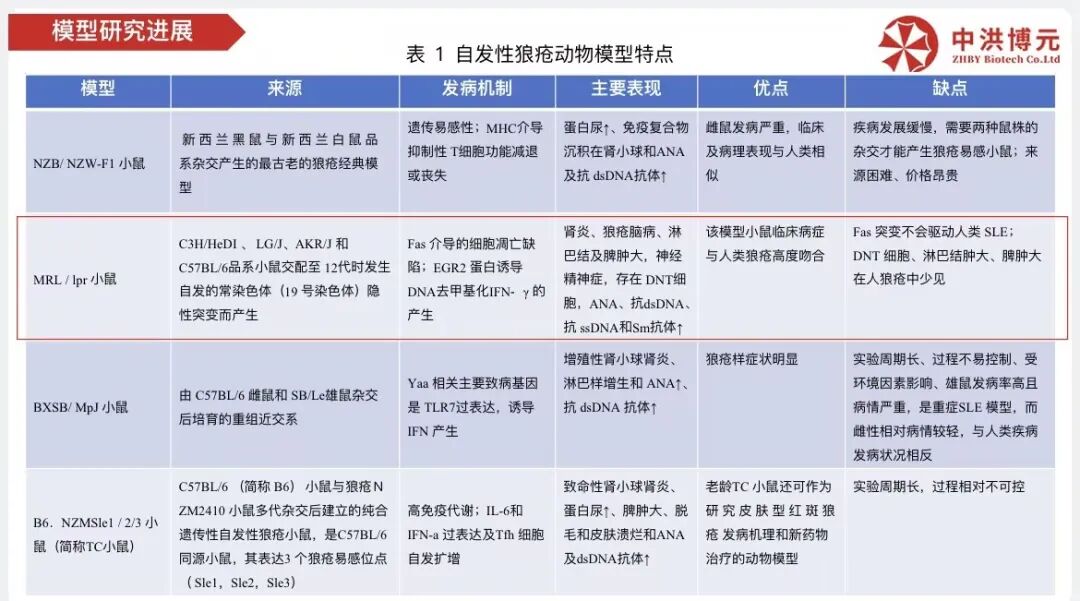
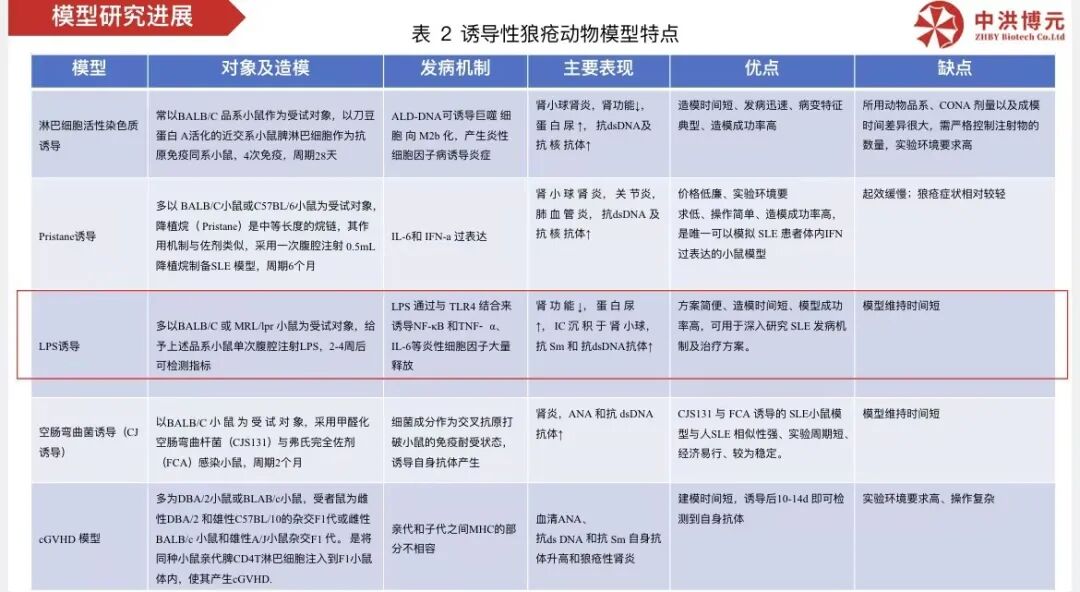
中洪博元——系统性红斑狼疮模型
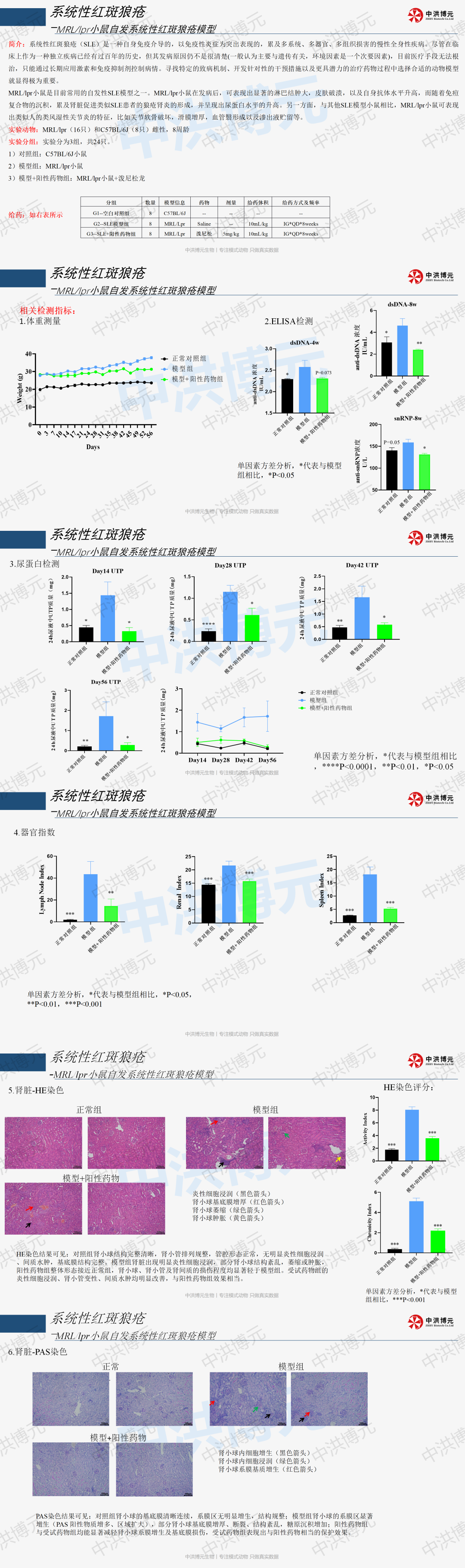
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
