银屑病治疗 “双线大捷”:《柳叶刀》认证口服多肽,外用新药重塑临床标准
银屑病(俗称 “牛皮癣”)作为全球高发的慢性免疫介导性炎症疾病,已困扰全世界近1.25亿患者。这种以皮肤红斑鳞屑为主要表现的疾病,常伴随银屑病关节炎、心血管疾病等并发症,严重影响患者生活质量。长期以来,银屑病临床治疗领域始终面临 “高效性与给药便利性难以兼顾、安全性与疗效持久性无法同步” 的核心困境;而自2025年起,创新口服多肽制剂icotrokinra与新型外用乳膏tapinarof的突破性研究成果,正从系统治疗与局部治疗双维度重塑银屑病的临床治疗。
图片来源:中洪博元
口服突破:icotrokinra 凭头对头优势登顶《柳叶刀》
2025年9月18日,《柳叶刀》发表的III 期临床试验(ICONIC-ADVANCE 1 & 2)结果,让创新口服多肽icotrokinra成为全球焦点。这款被《猎药人》评为2024 年度十大明星分子的药物,以 “靶向精准 + 口服便利 + 疗效卓越” 的三重优势,打破了系统治疗的现有瓶颈。

截图来源:The Lancet
Icotrokinra 的疗效优势在治疗早期即显现,第8周时便与安慰剂组拉开显著差距。至第16周,两项研究中 icotrokinra 组达到IGA 0/1分(皮损完全清除或几乎清除)且较基线改善≥2 级的患者比例分别高达68%和70%,而安慰剂组仅为11%和9%;更值得关注的是,55%~57% 的患者实现 PASI 90(病情改善至少90%),31%~32% 的患者达到PASI 100(皮损完全清除),这两项指标分别是安慰剂组的13倍以上和30倍以上。
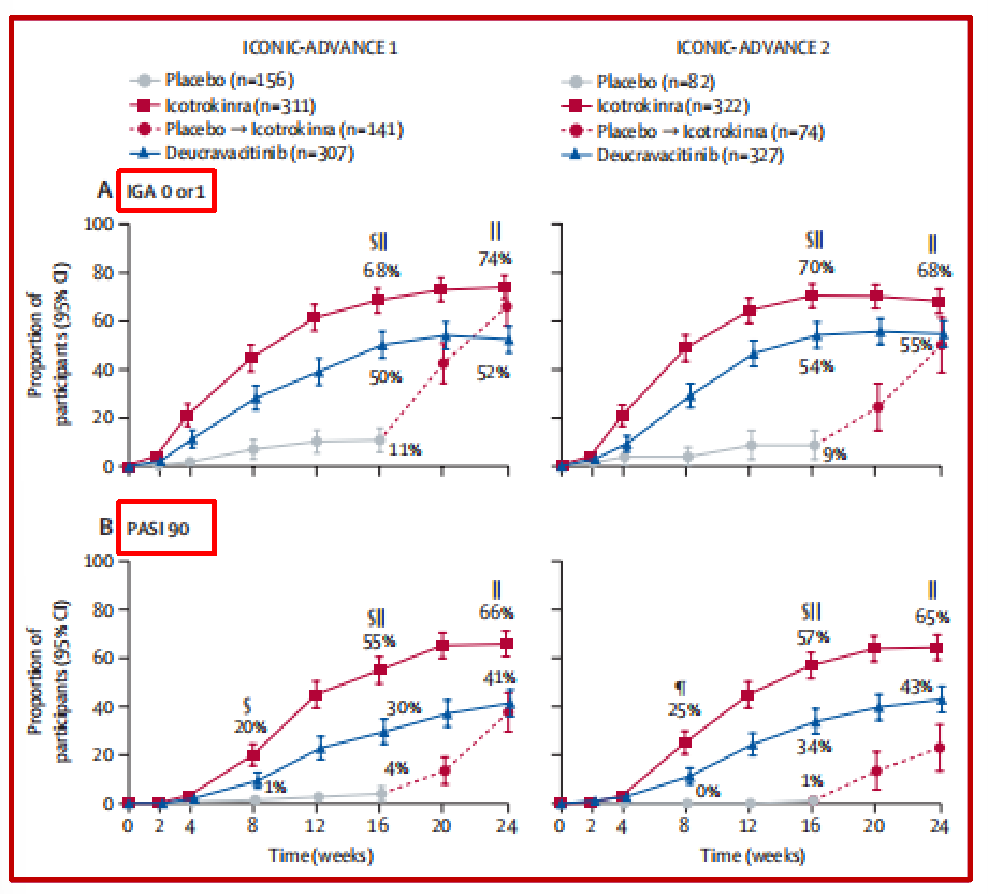
按治疗组划分的不同时间点达到共同主要终点IGA 0或1*及PASI 90的受试者比例 (图片来源:The Lancet)
注:IGA 为研究者整体评估,PASI 为银屑病面积和严重程度指数,“IGA 0或 1”指皮肤完全清除或几乎清除,“PASI 90”指病情较基线改善至少90%。
在与已获批口服药物 deucravacitinib 的头对头比较中,icotrokinra 的优势同样显著:第16周时其PASI 90应答率几乎是对照组的两倍(55%/57% vs 30%/34%),皮损完全清除率更是达到对照组的 3 倍左右(31%/32% vs 11%/14%),且这种优势持续至第24周。
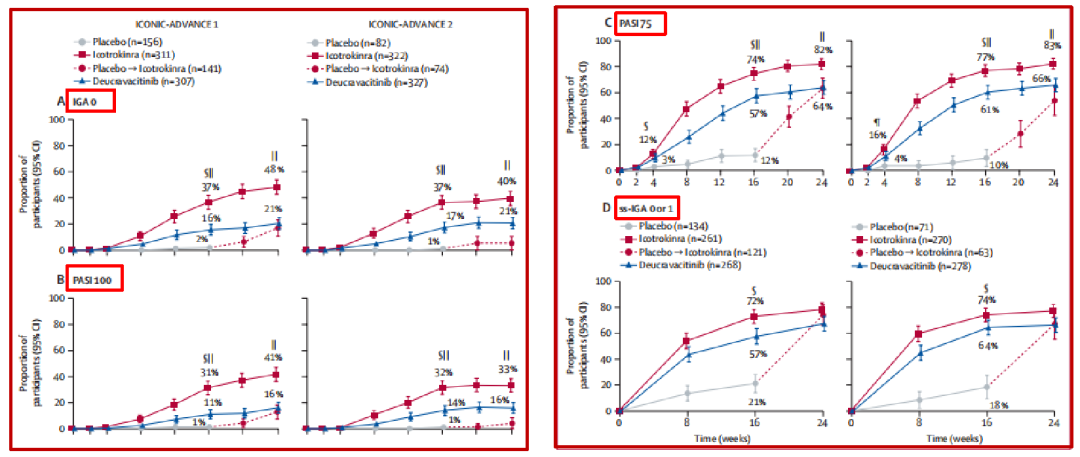
按治疗组划分的不同时间点达到 IGA 0、PASI 100、PASI 75及ss-IGA 0或1*的受试者比例(图片来源:The Lancet)
注:“IGA 0”指皮肤完全清除,“PASI 100”指银屑病病情较基线完全改善(改善100%),“PASI 75”指银屑病病情较基线改善至少75%,“ss-IGA”为头皮特异性研究者整体评估,“ss-IGA 0 或 1” 指头皮皮损完全清除或几乎清除。
外用革新:tapinarof 打破 25 年无新分子实体困局
在口服疗法取得突破的同时,外用治疗领域也迎来里程碑式进展。Dermavant Sciences公司的1% tapinarof 乳膏(美国商品名Vtama,中国通用名本维莫德)作为美国25年来首款获批的外用新分子实体,以 “全人群适用、无使用限制、非激素安全” 的特性,改写了外用治疗的临床规则。

图片来源:东方医药网
这款源自土壤线虫共生细菌代谢产物的天然化合物,属于 “first-in-class” 芳香烃受体(AhR)调节剂,其作用机制区别于传统外用药:通过调节AhR功能抑制IL-17介导的炎症反应 —— 这一通路正是银屑病治疗的 “明星靶点”,多款重磅生物制剂均靶向于此。得益于254 Da的小分子结构,tapinarof具有优异的皮肤渗透性,为其外用疗效提供了物理基础。
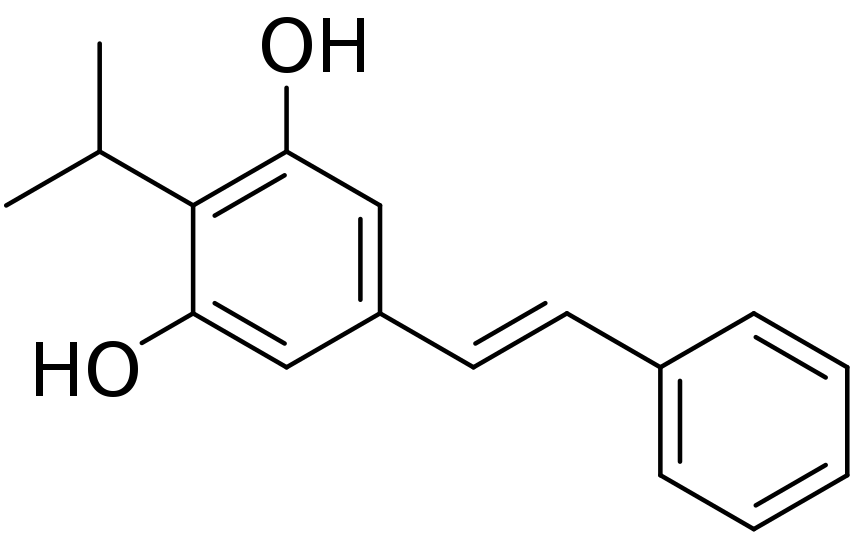
Tapinarof的分子结构式(图片来源:Edgar181, Public domain, via Wikimedia Commons)
tapinarof 的获批基于两项关键 III 期临床试验(PSOARING 1/2)的阳性结果:在接受治疗的患者中,36%~40%达到皮肤症状清除或接近清除标准,而对照组仅为6%(p<0.0001)。长期数据更显示出其独特优势:52周治疗期间疗效持续稳定,未出现疗法失效,且获得完全清除的患者停药后平均可维持疗效4个月。在患者满意度调查中,81.7%的受访者认为其优于既往使用的外用疗法(JAMA Dermatol, 2023)。
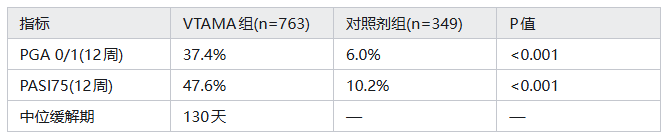
图片来源:NEJM Evidence
科研支撑与临床展望:从模型构建到疗法升级
创新疗法的突破离不开基础研究的支撑。建立稳定银屑病小鼠模型,可加速新药从实验室到临床的转化。从临床应用来看,icotrokinra与tapinarof的互补性为银屑病治疗提供了 “全域解决方案”:中重度患者可通过口服icotrokinra实现高效皮损清除,轻中度患者或维持治疗阶段可采用tapinarof外用,两种疗法均无需注射、安全性良好,有望显著提升患者长期治疗依从性。随着 ICONIC 系列研究的持续推进以及tapinarof适应症的拓展,银屑病治疗正从 “症状控制” 向 “持续缓解” 转变。对于全球上亿患者而言,这些创新疗法不仅意味着皮肤症状的改善,更有望降低并发症风险,重塑生活质量。正如Dermavant首席执行官Todd Zavodnick所言,以患者为中心的创新正在推动银屑病治疗进入 “高效、安全、便利” 三位一体的新时代。
中洪博元银屑病模型介绍——咪喹莫特乳膏诱导小鼠银屑病模型
咪喹莫特(IMQ)是一种咪唑喹啉胺类免疫调节剂(TLR7/8激动剂),能够诱导Balb/c小鼠、C57小鼠等背部皮肤发生银屑病样改变,其作用机制主要依赖于IL-23/IL-17轴,与人的银屑病发病机制非常相似,是目前使用最为广泛的银屑病样皮肤炎症急性小鼠模型。
选取健康雄性Balb/c小鼠,在完成规范适应性饲养后,通过专业处理构建皮肤暴露模型。实验采用 “预防性干预 + 同步治疗” 的科学方案:先进行3天预防性护理,随后在模型构建期间持续开展 7 天治疗,每日规范施加对应干预措施。实验中选用本维莫德乳膏作为阳性对照药物,采用每日两次外用涂抹的标准给药方式。
模型构建成功率达 100%,全程无小鼠死亡情况。
模型构建
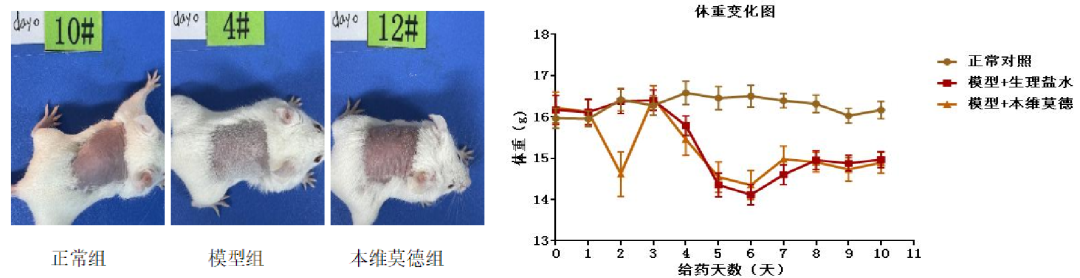
体重监测显示,实验结束时IMQ + 生理盐水(NS)组小鼠体重较空白对照组显著降低(P<0.01),而IMQ + 本维莫德(BWMD)组与IMQ+NS组无明显差异,提示造模对小鼠体重有影响但药物无此作用。
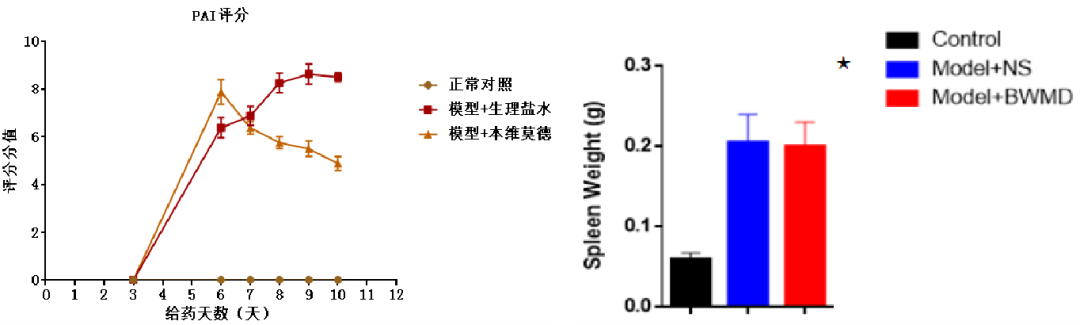
PASI评分结果表明,给药第7-11天,IMQ+NS组较空白对照组显著升高(P<0.01);给药第9-11天,IMQ+BWMD 组较IMQ+NS组显著降低(P<0.01)。取材当天对摘取小鼠脾脏,IMQ+NS组小鼠脾脏重量较空白对照组显著升高,模型组与阳性药物组无明显差异。
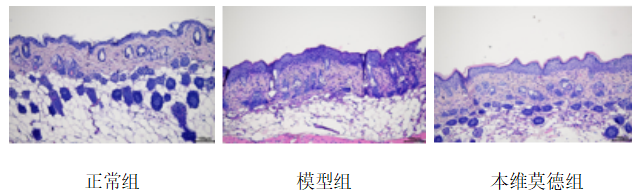
HE染色显示,空白对照组皮肤结构正常,IMQ+NS组出现明显角化不全、角化过度、棘层增厚及真皮层炎性细胞浸润、毛细血管扩张,IMQ+BWMD组上述病理改变明显减轻。
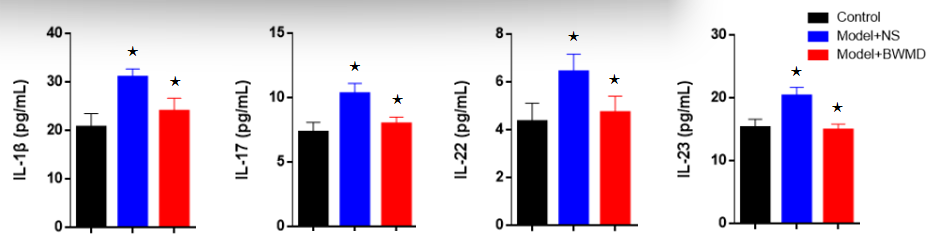
ELISA 检测结果显示,IMQ+NS组小鼠血清中 IL-1β、IL-17、IL-23、IL-22 水平较空白对照组显著升高(P<0.01),IMQ+BWMD 组较IMQ+NS组显著降低(P<0.01)。
综上,该模型能有效模拟银屑病病理特征及相关细胞因子变化,验证模型成立。
参考文献
【1】Gold, Linda Stein et al. “Once-daily oral icotrokinra versus placebo and once-daily oral deucravacitinib in participants with moderate-to-severe plaque psoriasis (ICONIC-ADVANCE 1 & 2): two phase 3, randomised, placebo-controlled and active-comparator-controlled trials.” Lancet (London, England) vol. 406,10510 (2025): 1363-1374. doi:10.1016/S0140-6736(25)01576-4.
【2】Bagel, Jerry et al. “Tapinarof cream 1% once daily for the treatment of plaque psoriasis: Patient-reported outcomes from the PSOARING 3 trial.” Journal of the American Academy of Dermatology vol. 89,5 (2023): 936-944. doi:10.1016/j.jaad.2023.04.061
【3】董颖颖,钟世玉,王琼等.银屑病小鼠模型建立的新方法[J].中国皮肤性病学杂志,2016,30(11),1127-1131.
