默沙东押注ADC赛道,sac-TMT成战略要点
2025年11月4日,默沙东宣布与黑石集团(Blackstone)就芦康沙妥珠单抗(Sacituzumab Tirumotecan,sac-TMT)达成协议,Blackstone向默沙东支付7亿美元,专项支持sac-TMT在2026年的部分研发成本,默沙东保留sac-TMT的开发、生产及商业化决策权与控制权,以sac-TMT未来部分收益权换取资金支持。

sac-TMT是2022年5月科伦博泰授权给默沙东的重磅抗体偶联药物(ADC)。随着默沙东的核心产品K药(Keytruda)专利悬崖临近,ADC药物成为其重要布局,但管线中其他ADC药物进展不及预期,如HER3-DXd 因未能突破全球III期临床关键终点,上市申请已被撤回,这也让sac-TMT更受到重视。
sac-TMT是一种靶向人滋养细胞表面抗原2(TROP2)的ADC,其设计原理是利用抗体精准识别并结合癌细胞表面高表达的TROP2蛋白,随后将强效的细胞毒性药物(拓扑异构酶I抑制剂KL610023)精准递送至肿瘤内部,从而最大限度地杀伤癌细胞,同时减少对正常组织的损伤。
全球首个获批的TROP2 ADC是吉利德(Gilead Sciences)的戈沙妥珠单抗(sacituzumab govitecan,Trodelvy),该药已在美国获批治疗TNBC、ER+/HER2-乳腺癌和尿路上皮癌(mUC)。2025年11月7日,吉利德宣布ASCENT-07 3期研究失利,Trodelvy一线治疗HR+/HER2-转移性乳腺癌未达到主要终点。此前,吉利德在推进Trodelvy用于治疗膀胱癌和针对既往接受过治疗的转移性非小细胞肺癌(NSCLC)中均遇到了困难。与Trodelvy相比,sac-TMT采用了一种独特的接头-有效载荷系统,以增强其稳定性和抗肿瘤活性,同时将肿瘤外毒性降至最低。
2024年11月27日,芦康沙妥珠单抗获NMPA批准上市,sac-TMT 不仅是首个获批上市的国产TROP2 ADC,也是中国首个获得完全批准的国产ADC。
另外,第一三共的德达博妥单抗(Dato-DXd)已在2024年3月份在国内申报上市,用于HR+/HER2-乳腺癌,预计2025年下半年获批。
在2025年ESMO大会上,sac-TMT一举拿下 2 项 LBA(含重磅主席论坛报告)和5项 poster,成为重磅报告最多的国产创新药之一。其与K药的联合方案在前列腺癌等领域打破K药治疗瓶颈,展现出强劲联合潜力。
2025年10月19日,中山大学肿瘤防治中心牵头的全国多中心III期临床研究OptiTROP-Lung04,成果发表于国际顶级期刊《新英格兰医学杂志》(NEJM)。

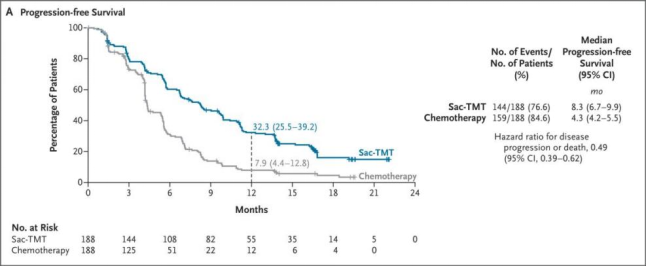
该研究纳入376例EGFR敏感突变、经EGFR-TKI治疗失败的局部晚期或转移性非鳞状非小细胞肺癌(nsq-NSCLC)患者,按 1:1 随机分配至 sac-TMT 组(5mg/kg,每2周一次)与培美曲塞联合卡铂/顺铂化疗组(每3周一次,4周期后培美曲塞单药维持),中位随访时间18.9个月,主要研究终点为盲态独立评审委员会(BIRC)评估的无进展生存期(PFS),关键次要研究终点为总生存期(OS)。
结果显示,sac-TMT 组中位无进展生存期(PFS)达8.3个月,显著优于化疗组的4.3个月(HR=0.49,95% CI: 0.39–0.62,P<0.0001),疾病进展或死亡风险降低 51%,成为全球首个TROP2 ADC单药治疗该人群中实现 PFS显著获益的III期研究。在总生存期(OS)等关键指标上,sac-TMT 也呈现出具有统计学意义和临床意义的改善。
截至目前,sac-TMT已在中国获批3项适应症,分别用于治疗既往至少接受过2种系统治疗的不可切除的局部晚期或转移性TNBC、经EGFR-TKI治疗后进展或经EGFR-TKI和含铂化疗治疗后进展的EGFR基因突变阳性的局部晚期或转移性nsq-NSCLC。
肺癌是我国第一大恶性肿瘤,据统计,我国每年新发肺癌患者达106万。肺癌的病理分型主要包括非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC),其中NSCLC最常见,约占所有肺癌患者的80%-85%。EGFR突变晚期NSCLC首选EGFR-TKI治疗;EGFR-TKI治疗耐药后以含铂双药化疗为基础的治疗方案是目前主要的标准治疗手段。但现有的治疗方案疗效欠佳,尤其是在延长患者总生存期上,存在较大未被满足的临床需求。
PD-1/VEGF双抗在该赛道十分火热,康方生物自主研发的依沃西单抗布局快速且广泛,在中国已获批用于治疗EGFR-TKI治疗进展的局部晚期或转移性nsq-NSCLC及PD-L1表达阳性的晚期NSCLC,并于2025年正式进入医保,sac-TMT作为ADC单药治疗能够和PD-1/VEGF双抗竞争一定的市场实属难得。
此外,sac-TMT用于治疗既往接受过内分泌治疗且在晚期或转移性阶段接受过其他系统治疗的不可切除的局部晚期或HR+/HER2-转移性乳腺癌的上市申请已获CDE受理,并被纳入优先审评审批程序。
当前,默沙东已围绕 sac-TMT 在肺癌、乳腺癌、胃癌、妇科肿瘤等多个领域开展15项III期全球性临床研究。2027年起该药将迎来9项III期临床试验数据的集中披露,有望进一步拓展适应症范围。
黑石集团作为全球顶尖私募机构,凭借丰富的临床与商业经验已助推 200 余种药物上市。此次主动参与sac-TMT专项融资,充分体现了对其商业价值的高度认可。在默沙东的全力推动与黑石集团的资金支持下,sac-TMT必将加速冲击全球重磅药物阵营,其广阔的市场前景值得期待。
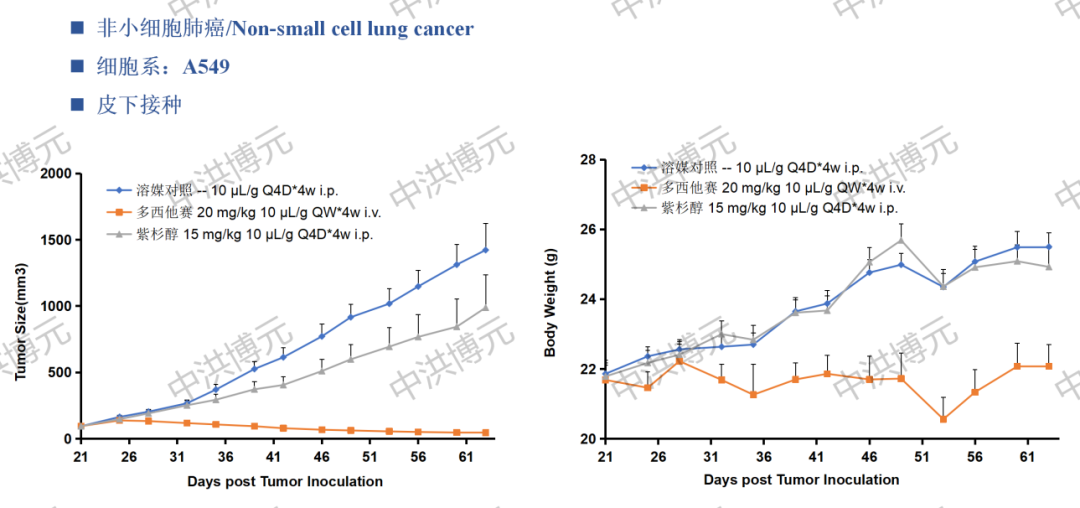
中洪博元CDX模型
已验证肺癌细胞系:NCI-H1975、A549、Calu-3、LLC 、PC-9、NCI-H838、HCC827、NCI-H69、NCI-H1650、NCI-H1299、Calu-1。
部分数据展示:
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司专业从事药物研发临床前CRO服务,公司构建了从疾病模型制备→药效药理→病理检测→生化检测→结果报告一体化服务。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。中洪博元药理药效筛选评价平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。

中洪博元成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
如想了解实验详情欢迎咨询:
💬 微信公众号「中洪药效评价」咨询
📞 拨打15180153675(微信同号)
🔗 官网https://www.zhbyind.com/
